併用療法が承認済みの場合、合剤承認に基づく合剤特許の存続期間延長は可能か?: 知財高裁平成17年(行ケ)10012
【背景】
原告は抗ウィルス薬ラミブジン及びそれと他の抗ウィルス薬との併用剤に関する特許の特許権者であり、ラミブジンとジドブミンとの合剤(販売名コンビビル錠)の薬事法上の承認を得たことに基づき同特許の存続期間延長登録の出願をしたが拒絶審決を受けたため審決取消訴訟を提起した。
審決理由は下記のとおり。
(1)ラミブジンが、ジドブミンとの併用を用法・用量として、かつ、併用療法を効能・効果として既に承認されていることから、本出願に係るものと先の承認の対象となったものとの違いは、単に、単剤を併用するか、又は合剤にするかの違いに過ぎず両者は実質的に同一であるため、特許発明を実施することが出来なかったという要件(特67条の3第1項1号)を満たしていない。
(2)原告提出の資料からでは、米国治験計画書の提出日から我が国での製造承認の日までの間、必要な手続きが引き続いてされていたものとは直ちには認めることができないから、請求人(原告)が請求する特許発明の実施をすることができなかった期間が適切であるということが出来ない。
【要旨】
存続期間の延長制度の趣旨及び特68条の2の文言に照らせば、期間延長後の特許権の効力は、当該品目に限定されず、成分により特定される「物」及び効能、効果により特定される「用途」について特許発明を実施する場合全般に効力が及ぶものとし、それ以外には効力は及ばないとしたものであると解される。
そうすると、当該処分の対象である成分により特定される「物」と当該処分で定められた「用途」によって画される範囲において特許発明が実施できるようになっているというべきであるから、その物の使用の形態等に変更があるため、重ねて同様の処分を受けることが必要であるとされていても、「特許発明の実施に67条2項の政令で定める処分を受けることが必要であった」と認めることはできないと解するのが相当である。
本件において、先の承認は、実質的には、今回の承認に係る承認書の有効成分の欄に記載されているラミブジンと既に先の承認により製造承認を受けているエピビル錠の有効成分であるジドブジンの両方を有効成分とする抗ウィルス剤の製造承認と同一視できるものというべきである。
従って、ラミブジンとジブドミンの両方の有効成分の併用という形態を、その両者を組み合わせた錠剤にするため、すなわち剤形の変更のため、改めて薬事法上の製造承認を受ける必要があったからといって、「特許発明の実施に67条2項の政令で定める処分を受けることが必要であった」と認めることはできないと判示した。
請求棄却。
【コメント】
裁判所は、「期間延長後の特許権の効力は、用法、用量、使用方法等を特定した具体的な品目に限定されず、有効成分により特定される「物」及び効能,効果により特定される「用途」について特許発明を実施する場合全般に効力が及ぶものとし,それ以外には効力が及ばないとしたものであると解される。」としているが、そもそも特許権の効力を規定する特68条の2に規定されている「処分の対象となった物」及び「特定の用途」が、そのまま登録要件に適用すること、さらにそれぞれ製造承認書中の「有効成分」及び「効能・効果」によってのみ特定されると解釈する根拠は乏しい。
この点については、後の下記裁判でも争点となり、知財高裁において一応の判断が出されている。
また、被告である特許庁は訴訟の中で、海外での臨床期間の算入の要件について下記のように言及している。
我が国での医薬品の製造承認申請に外国における治験の結果等を使用した場合には、(1)そもそもその外国における治験が我が国で承認を得ることを目的としていたものであることが必要であり、かつ、(2)外国で承認申請をした者が我が国で承認申請をした者と同一であるか、あるいはその意思を受けて治験を行ったものであって、その後遅滞なく我が国における承認申請を行ったものであること、が必要となる。
言い換えれば、外国での治験及び承認は我が国における承認を得るための手続の一部として我が国における手続と継続性を有するものである必要がある。
この点については裁判所の判断はされていない。
コンビビル錠(Combivir tablets):
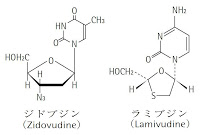
グラクソ・スミスクライン(GlaxoSmithKline)が販売する抗ウイルス化学療法剤(有効成分としてジドブジン(Zidovudine)とラミブジン(Lamivudine)を含有する合剤)であり、HIV感染症を効能・効果とする。

コメント
本件においては確か物質特許が対象だったと思いますが、合剤特許が対象であっても同じ結論だったのでしょうねえ?
ところで、既承認用途Aの薬剤Xと、既承認用途Bの薬剤Yを組み合わせて、用途AでXとYの合剤の承認を取得したら、Yの物質特許、XとYの合剤特許は延長されるのでしょうか?
ぎっちょんさん、コメントありがとうございます。
YのA用途発明、またはX及びYの併用(合剤)用途の発明の実施にとって承認を得る必要があったことを合理的に主張できれば、存続期間延長可能な気がします。
合剤承認前であったとしても、薬剤Yが薬剤Xと同時に使われることが実際可能だったのかどうか(off-label useも含めて)、という点が気になりますが。
ところで、2008年1月23日に特許庁が公表した「イノベーションと知財政策に関する研究会 検討資料」
(URL: http://www.jpo.go.jp/shiryou/toushin/kenkyukai/pdf/innovation_wg_01_shiryou/shiryou04.pdf)
の資料41ページには、興味深い記述として、下記について法改正と審査基準の見直しを行っているとあります。延長登録制度については不明点が多く、医薬業界全体にとって今後良い方向へ制度が改善されていくことを望みます。
・特許権存続期間の延長制度の在り方
(対象の拡大(例、遺伝子組換え生物)、DDSなど剤型の保護など、制度の在り方について、特許法68条の2に物と用途に加え、剤型も対象とするか否か。施行令3条の対象を拡大するべきか否か。)