レバミピドの用途特許: 知財高裁平成20年(行ケ)10366
【背景】
 大塚製薬が有する「胃炎治療剤」に関する特許(第2812998号)の無効審決(無効2007-800196号)取消訴訟。
大塚製薬が有する「胃炎治療剤」に関する特許(第2812998号)の無効審決(無効2007-800196号)取消訴訟。
争点は進歩性。
引用発明との相違点は、本件特許発明が「胆汁酸の胃内への逆流に起因する胃炎」の治療剤であるのに対し、引用発明は「胃潰瘍」治療剤である点だった。
請求項1:
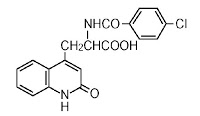
2-(4-クロルベンゾイルアミノ)-3-(2-キノロン-4-イル)プロピオン酸またはその塩を有効成分とする,胆汁酸の胃内への逆流に起因する胃炎の治療剤。
【要旨】
裁判所は、
「本件出願前に,「胃潰瘍治療剤」としての薬効が知られている場合,当業者が,「胃炎治療剤」としての薬効も存在するとの技術思想に容易に想到し得たか否かは,
①「胃潰瘍」と「胃炎」の病態・発症機序における相違の有無,
②「胃潰瘍治療剤」と「胃炎治療剤」の作用機序における相違の有無,
③「胃潰瘍治療剤」と「胃炎治療剤」の双方に効果のある他の薬剤の比較,検討,
④本件化合物の胃炎治療への適用を阻害する要素の有無等
を総合的に考慮して判断すべきである。」
と述べ、上記観点から下記のとおり検討した。
1. 「胃潰瘍」と「胃炎」の病態・発症機序及び「治療剤」の作用機序等の相違の有無について
裁判所は、
「本件出願当時,当業者においても,胃潰瘍と胃炎とが病態・発生機序において異質であり,その治療剤の作用機序が異なるとの認識をもっていたとは認め難い。」
と判断した。
原告は、
「国民衛生の動向(甲55)においても,胃潰瘍患者と胃炎患者とが別異に分類されており,医療現場においても区別して取り扱われていることや,医薬品の製造承認において胃潰瘍治療剤と胃炎治療剤が区別されていることを根拠として,胃潰瘍と胃炎の治療剤のそれぞれの作用機序が異なる」
と主張した。
しかし、裁判所は、
「胃潰瘍と胃炎が別個の疾患として区別されているからといって,胃潰瘍治療剤と胃炎治療剤の作用機序の相違を示すことにはならず,また,胃炎に対する治療効果を妨げる理由にもならない。」
と判断した。
2. 「胃潰瘍治療剤」と「胃炎治療剤」の双方に効果のある他の薬剤の検討
裁判所は、
「本件化合物以外の多様な化合物又は医薬品について,胃潰瘍治療剤としての用途と併せて胃炎治療剤としての用途が記載されており,それらの化合物又は医薬品と本件化合物とが別個の性質を有し,胃炎に対する作用機序が異なることを認めるだけの根拠はない。」
とした。
これに対し、原告は、
「上記文献では,胃潰瘍治療剤には胃炎治療剤としての用途を有するものもあるが,そうでないものも多いから,胃炎としての用途に想到することが容易とはいえない」
と主張した。
しかし、裁判所は、
「そのような胃潰瘍治療剤が存在したとしても,前記のとおり,胃潰瘍治療剤の中に胃炎治療剤としての用途を有するものが多数存在する以上,当業者が胃潰瘍治療剤である本件化合物について胃炎治療剤への用途を予測することが困難であったということはできない。」
と判断した。
3. 「胆汁酸の胃内への逆流に起因する胃炎」との用途について
裁判所は、
「全証拠によっても,胃炎治療剤については,胆汁酸の胃内への逆流による胃炎と胃炎一般を区別すべきであるとする医学的,薬学的知見も見当たらない。以上によれば,当業者は,胃潰瘍治療剤である本件化合物が胆汁酸の胃内への逆流による胃炎治療剤としての用途をも有することを予測することができたということができる。」
と判断した。
4. 阻害要因の存在について
原告は、
「本件化合物にはPGE2を生成する作用があり,PGE2には炎症惹起作用があるから,これを胃炎治療剤としての用途に用いることには阻害要因がある」
と主張した。
しかし、裁判所は、
「本件特許発明の出願当時,PGE2の炎症時における化学媒介物質としての作用が知られていたとしても,~同時期にPGE2の胃粘膜保護作用を指摘する文献も多く刊行されていることなどにかんがみると,炎症時の化学媒介物質としての作用の指摘は,胃炎への用途を考えるについての阻害要因とはならない。~以上を総合すれば,一部にPGE2の胃粘膜保護作用を否定する文献やPGE2の炎症惹起性を肯定する文献があることは,本件化合物について胃炎への用途を想起することの阻害事由とはならない。」
と判断した。
5. 顕著な薬理効果について
原告は、
「シメチジンを比較対象薬物として本件明細書の薬理実験1と同様の実験をしたところ,本件化合物の抑制率が77%であったのに対し,シメチジンの抑制率は2%であったから(甲18),顕著な薬理効果がある」
と主張した。
しかし、裁判所は、
「①本件明細書には,本件化合物の抑制率が77%であるとの記載はあるものの,その記載のみをもって,本件特許発明をすることが容易ではなかったことの根拠として評価することができるかは疑問であること,②シメチジンより酸分泌抑制効果に関して内視鏡改善度の高い胃炎治療剤が複数存在すること(甲56)に照らし,シメチジンとの比較のみで顕著な効果が示されたとすることができるかは疑問であること等によれば,本件特許発明が従来技術からは予測し得ない程度の効果を奏し得たとはいえない。」
と判断した。
請求棄却。
【コメント】
本件について裁判所の示した基準を参考にすると、同一化合物について「X治療剤」としての薬効が知られている場合、当業者が「Y治療剤」としての薬効も存在するとの技術思想に容易に想到し得たか否かは下記項目等を総合的に考慮して判断する必要がある。
①「X」と「Y」の病態・発症機序における相違の有無
②「X治療剤」と「Y治療剤」の作用機序における相違の有無
③「X治療剤」と「Y治療剤」の双方に効果のある他の薬剤の比較、検討、
④本件化合物のY治療への適用を阻害する要素の有無
「X」と「Y」とが別個の疾患として区別されているからといって、「X」治療剤と「Y」治療剤の作用機序の相違を示すことにはならない。
本件に関して、比較例とすべき複数の胃炎治療剤が存在するにもかかわらず、シメチジンとの比較のみで顕著な効果が示されたと主張することには無理があった。
本件特許は大塚製薬の胃炎・胃潰瘍治療剤ムコスタ(Mucosta、一般名: レバミピド(Rebamipide))の用途に関するもの。
特許権の存続期間は2009年8月14日に満了しており、多数の後発品が既に参入している。
参考:
- 沢井製薬 press release: 2009.10.15 レバミピド製剤の特許訴訟終結に関するお知らせ


コメント