レナリドミドとデキサメタゾンの組合せ医薬: 知財高裁平成24年(行ケ)10124
【背景】
「癌および他の疾患を治療および管理するための免疫調節性化合物を用いた方法および組成物」に関する特許出願(特願2004-505051、特表2005-530784、WO2003/097052)の拒絶審決(不服2009-7935号)取消訴訟。
争点は進歩性。
本件補正発明:
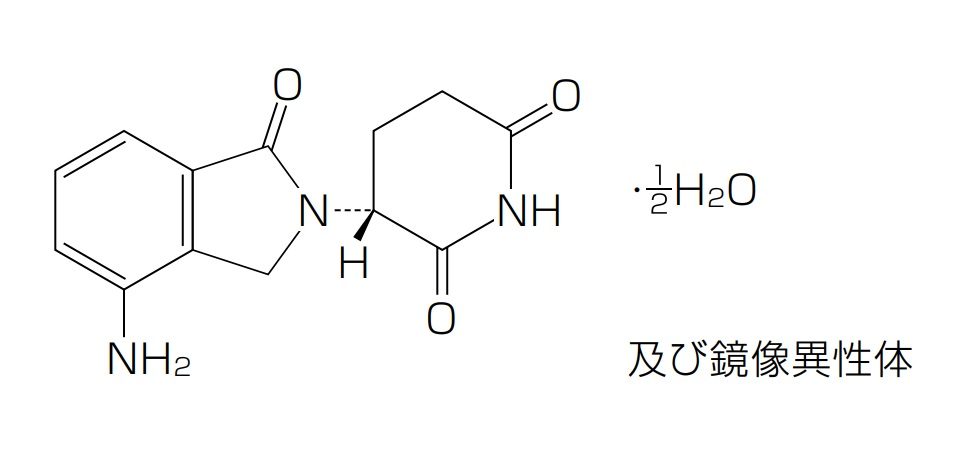
治療上有効な量の化合物3-(4-アミノ-1-オキソ-1,3-ジヒドロ-イソインドール-2-イル)-ピペリジン-2,6-ジオンまたはその製薬上許容される塩,溶媒和物もしくは立体異性体,および治療上有効な量のデキサメタゾンを含む多発性骨髄腫の治療のための組合せ医薬であって,該化合物は多発性骨髄腫を有する患者に1~150mg/日の量で周期的に経口投与され,該デキサメタゾンは該患者に周期的に経口投与される,上記組合せ医薬
本件審決が認定した引用発明並びに本件補正発明と引用発明との一致点及び相違点は以下のとおり。
引用発明:
IMiD1,IMiD2あるいはIMiD3のいずれかであるサリドマイドアナログ及びデキサメタゾンを含むヒト多発性骨髄腫細胞の増殖の抑制のための組合せ
一致点:
サリドマイドアナログ及びデキサメタゾンを含むヒトの多発性骨髄腫の抑制のための組合せである点
相違点1:
本件補正発明の組合せにおいては,デキサメタゾンと組み合わされるサリドマイドアナログが「3-(4-アミノ-1-オキソ-1,3-ジヒドロ-イソインドール2-イル)-ピペリジン-2,6-ジオン)又はその製薬上許容される塩,溶媒和物もしくは立体異性体」(本願化合物)であるのに対し,引用発明においては,「IMiD1,IMiD2あるいはIMiD3のいずれか」である点
相違点2:
本件補正発明の「組合せ」には,本願化合物及びデキサメタゾンがそれぞれ「治療上有効な量」含まれ,また,「多発性骨髄腫の患者」に投与される「多発性骨髄腫の治療のための組合せ医薬」であるのに対し,引用発明の「組合せ」は,「ヒト多発性骨髄腫細胞」に対して投与される「多発性骨髄腫の抑制のための組合せ」であって,本願化合物及びデキサメタゾンがそれぞれ「治療上有効な量」含まれる点の特定がなされていない点
相違点3:
本件補正発明においては,本願化合物が「1~150mg/日の量で周期的に経口投与され」,また,「デキサメタゾン」が「周期的に経口投与さ れる」のに対し,引用発明においては,これらの点の特定がなされていない点
【要旨】
主 文
1 原告の請求を棄却する。
2 訴訟費用は原告の負担とする。
3 この判決に対する上告及び上告受理の申立てのための付加期間を30日と定める。
裁判所の判断(抜粋)
(1) 相違点1について
原告は,仮に,引用例に記載されたIMiD1ないし3のうちの1つは,本願化合物に相当することが認識できるとした場合も,実際には,これら3種の化合物のうち,いずれが本願化合物であるかが特定できない場合には,当業者は,引用発明から本件補正発明に到達する試みをしたはずであるとはいえず,引用例には,IMiD1ないし3の3種の化合物のうちのいずれが本願化合物であるかについての示唆はないから,引用発明の記載に基づいて,当業者が本願化合物を容易に選択し得たとはいえないと主張する。
しかし,引用例には,IMiD1ないし3のそれぞれをデキサメタゾンと組み合わせた結果が個別に記載されているのであるから,当業者は,引用例の記載から,本願化合物を含む上記3種の化学構造式のサリドマイドアナログのそれぞれとデキサメタゾンとの組合せが,多発性骨髄腫の抑制のために有用であると理解することができる。
したがって,本願化合物とデキサメタゾンとを組み合わせた多発性骨髄腫の抑制のための組合せ自体が引用例に記載されていることは明らかであり,引用例に,IMiD1ないし3の3種の化合物のうちのいずれが本願化合物であるかについての特定や示唆がなくても,当業者であれば,本願化合物を容易に選択し得たものということができる。
(2) 相違点2について
引用発明のIMiD1ないし3の3種のいずれかとデキサメタゾンとからなる組合せについてのインビトロ試験は,多発性骨髄腫の患者に投与する多発性骨髄腫の治療のための組合せ医薬とすることを念頭において行われたものであることは明らかであるから,インビトロ試験に用いられたそれぞれの組合せを,多発性骨髄腫の患者に投与する多発性骨髄腫の治療のための組合せ医薬とすることは当業者が容易に行い得ることである。そして,その際に,それぞれの医薬成分を治療上有効な量含むものとすることも,当業者が当然に行うことであるというべきである。
(3) 相違点3について
医薬の投与に際し,毒性や副作用等が問題とならない範囲において所望の治療効果が得られるように必要な投与量や投与周期を設定することは当業者が通常行うことであるし,引用例においては,本願化合物と化学構造の類似したサリドマイドを多発性骨髄腫の治療のために患者に1日当たり100~800mg の範囲(平均400mg)で投与したことも具体的に記載されているのであるから,IMiDsの薬理作用がサリドマイドよりも優れることを示す試験結果も考慮して,引用発明における組合せを多発性骨髄腫の患者に治療のために「経口」投与剤とする際に,本願化合物の投与量を本件補正発明で規定する範囲で周期的に投与するものとし,また,デキサメタゾンを周期的に投与するものとすることは当業者が容易になし得ることである。
(4) 作用効果について
原告は,甲15等は,本件補正発明により達成された予想外の結果を確認するものであると主張する。しかし,甲15等に示される効果は,いずれも本願明細書の記載から推論できる範囲を超えたもの,あるいは本件補正発明の効果であるとは直ちには認めることのできないものであるから,原告の主張は,本願明細書の記載に基づかないものであり,これを採用することはできない。
原告は,レナリドミドを有効成分として含有する Revlimid の商業的成功は,本件補正発明の進歩性を裏付けるものである旨主張する。
しかし,医薬の商業的成功は,製品の技術的特徴だけでなく,価格設定,宣伝,需要動向等の要因が密接に関連するものであり,原告が挙げる Revlimid の売上げが多大なものであるとしても,それが本件補正発明が進歩性を有することを裏付けるものということはできない。
【コメント】
原告が提出した甲15等に基づく作用効果についての原告主張を裁判所は採用しなかった。進歩性を主張するための、いわゆる後出しデータの参酌が許されるかどうかのラインについて、裁判所の判決内容はクリアではなかった。
ところで、審決は、その作用効果についての原告の主張を下記のように判断している。
請求人の主張する実施例6.5.6(段落【0209】)には、「再発したまたは不応性の多発性骨髄腫の治療」として、「メルファラン(50mg、静脈内、本発明の免疫調節性化合物(約1~150mg、経口、毎日)、およびデキサメタゾン(40mg/日、経口、1~4日目)を併用して4サイクルまで4~6週間ごとに治療を施した。本発明の免疫調節性化合物を毎日およびデキサメタゾンを毎月投与することよりなる維持療法を、疾患進行の間、継続させた。」ことが記載され、「メルファランおよびデキサメタゾンと組み合わせて本発明の免疫調節性化合物を用いた療法は、非常に活性が高く、一般的には、他の方法では予後不良である極度の前治療の施された多発性骨髄腫患者で許容されるものであった。」と記載されている。
ここで、上記段落には、「本発明の免疫調節性化合物」が具体的にどのような化学構造を有しているのか記載されていないところ、「本発明の免疫調節性化合物」に関しては、本願明細書の段落【0027】~【0052】に詳述され、代表的な化合物に関し、段落【0031】に一般式I(化学式は省略する)の化合物が、段落【0035】に一般式II(化学式は省略する)の化合物が、段落【0049】に一般式III(化学式は省略する)の化合物がそれぞれ記載されているように、「本発明の免疫調節性化合物」には、多くの化合物群が包含されている。
してみると、実施例6.5.6において多発性骨髄腫の治療のために患者に投与されている免疫調整性化合物が、(現在の請求項1に特定された)本願化合物を当然に意味するものとは認められない。そして、当該段落の記載が本願化合物を使用した組合せ医薬による治療結果を示すものであると直ちには認めることもできないから、本願補正発明の効果は本願明細書の記載からは明らかとはいえない。
また、仮に、実施例6.5.6において多発性骨髄腫の治療のために患者に具体的に投与されている免疫調整性化合物が本願化合物であるとしても、上記実施例においては、組合せ医薬を使用した場合の効果に関して、「非常に活性が高く」、「極度の前治療の施された多発性骨髄腫患者で許容されるものであった。」と、定性的に記載されているに過ぎず、従来からの療法に比べて組合せ医薬が具体的にどの程度優れているのかを当業者は理解できないところ、本願化合物とデキサメタゾンを含む組合せ医薬が再発したあるいは不応性の患者に対し有効である点の効果が引用例から予測される範囲内のものであることは本願補正発明の効果についての検討においてすでに述べたとおりであるから本願補正発明の効果は格別なものとはいえない。
参考:
本件には分割出願が多数存在している。
- 特願2006-288966(特開2007-008966)拒絶査定不服審判(決定却下): 肺癌または強皮症用途
- 特願2009-116363(特開2009-191072)拒絶査定不服審判(係属中):非ホジキンリンパ腫(NHL)用途
- 特願2012-273326(特開2013-049734)出願審査請求済み: 非ホジキンリンパ腫(NHL)用途
- 特願2009-116367(特開2009-173683)拒絶査定不服審判(係属中):多発性骨髄腫用途
- 特願2013-038222(特開2013-126999)出願審査請求済み: 多発性骨髄腫用途
抗造血器悪性腫瘍剤のレブラミド®カプセル(Revlimid®Capsules)(一般名:レナリドミド水和物(lenalidomide)は、米国Celgene Corporationが創製した免疫調節薬(IMiDs)。セルジーン(株)が製造販売している。同社は、再発又は難治性の多発性骨髄腫に対して、レナリドミドとの併用で用いる経口デキサメタゾン4mg製剤(レナデックス®錠4mg)についての製造販売承認申請もレナリドミドと同時期に行い、2010年6月に承認を取得している。


コメント