 *Case2019
*Case2019 2019.07.25 「シオノケミカル v. イコス」 特許庁審決 無効2017-800140号事件
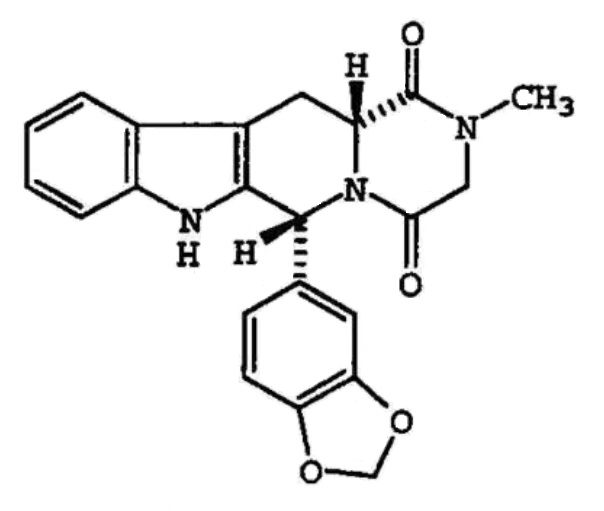
タダラフィルの特定用量製剤(シアリス®錠)特許: 特許庁審決 無効2017-800140号事件イコス・コーポレイションが保有する「単位製剤」に関する特許(第4975214号; 存続期間満了日2020.4.26)に対してシオノケミカル(株)が請求した無効審判。審判合議体は、訂正を認めたうえで、本件発明1~13は無効理由2(進歩性欠如)により無効にすべきものであると判断した。訂正後の請求項1(本件発明...