Law360からの情報によると、2019年12月30日、大鵬薬品は、Natco社によるLonsurf®のANDA(paragraph IV certification)に対して特許侵害であると主張して、デラウェア州連邦地裁に訴訟を提起したようです(2019.12.30 「Taiho Pharmaceutical Co., Ltd. et al v. Natco Pharma Ltd. et al」US District Court for the District of Delaware 1:2019-cv-02368)。
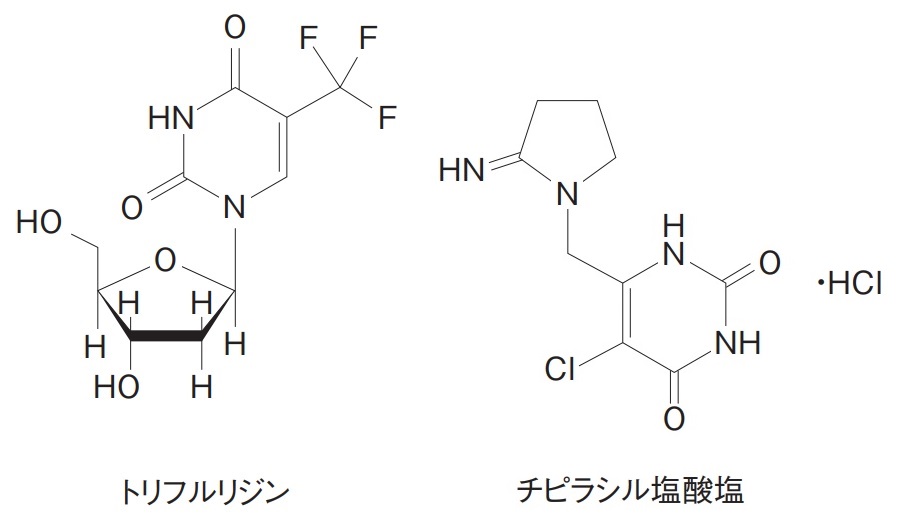
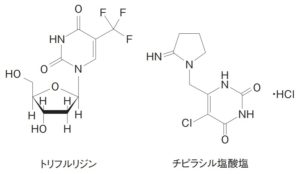
抗悪性腫瘍剤ロンサーフ(Lonsurf)®配合錠は、有効成分としてトリフルリジン(Trifluridine (FTD))及びチピラシル塩酸塩(Tipiracil hydrochloride (TPI))を1:0.5のモル比で配合した経口ヌクレオシド系抗悪性腫瘍剤。FTDは本剤の抗癌活性成分であり、経口投与することで直接DNAに取り込まれてDNA機能障害を起こすことで抗腫瘍効果を示すと考えられている。TPIはFTDの分解酵素であるチミジンホスホリラーゼ(TPase)を特異的に阻害することにより、FTDのバイオアベイラビリティを高めることを可能にしている。2014年に世界に先駆けて日本で発売。米国においては、2015年9月22日に承認され、大鵬薬品の米国子会社である大鵬オンコロジー社が販売。親会社の大塚ホールディングスの決算資料によると、2018年度の北米でのLonsurf®の売上は200億円、2019年度では225億円を計画している(大塚ホールディングス2019年度第3四半期決算補足資料(2019年11月12日発表))。
Lonsurf®のOrangebookに収載されている米国特許群は以下のとおり。なお、特許権者は、5,744,475特許、6,479,500特許及び7,799,783特許について、Lonsurf®の承認(2015年9月22日)に基づくPTEを2015年11月19日に出願し、認められればそのうちどれか一つをPTEとして選択するという特許延長審査戦略をとった。そのうち、5,744,475特許はTPIを保護する物質特許であり、1996.3.28出願、1998.4.28登録、PTAなし、2015.12.29にPTE出願は特許権者により自主的に取下げられ、2016.3.28満了となっている。
- 6,479,500・・・TPI投与により抗癌剤による副作用を軽減する方法特許。2000.3.16出願、2002.11.12登録、PTAなし、PTE出願は特許権者により自主的に取下げられ(2017.8.3)、2020.3.16に満了する。
- RE46,284・・・FTDとTPIの特定用法用量で消化器癌と乳癌を治療する方法特許。2005.1.26出願、7,799,783特許登録(2010.9.21)、PTAが688日、reissue請求し(2015.12.20)、RE46,284特許として登録(2017.1.24)、特許権者は7,799,783特許のPTEをRE46,284特許に転用するよう特許庁に請求している(2017.4.20)。7,799,783特許のPTEについてのUSPTO宛FDA Final Eligibility Letterは2018.10.10発せられている状況。Orangebook上では、満了日は2026.12.16のままであり、PTE付与反映には至っていないようである。
- 10,456,399・・・FTDとTPIの特定用法用量で腎障害を伴った癌患者を治療する方法特許。満了日は2037.2.3(20年)。
- 9,527,833・・・TPIの特定結晶形特許。満了日は2034.6.17(20年)。
- 10,457,666・・・TPIの特定結晶形特許。満了日は2034.6.17(20年)。
参考:
- 2020.01.03 Natco Pharma press release: NATCO files ANDA for Trifluridine/ Tipiracil Hydrochloride Tablets for the USA market

コメント