>関連判決②から続く
1.背景
ジェネリックメーカー各社(共和薬品工業、ニプロ、東和薬品及びMeiji Seikaファルマ)が抗精神病薬エビリファイ®の医薬用途特許(第4178032号)に対して各々請求した特許無効審判事件において、特許庁は、エビリファイ®の「うつ病・うつ状態」の効能・効果を保護する請求項2に係る発明についての無効の主張を退けたが、エビリファイ®の「双極性障害における躁症状」の効能・効果を保護する請求項1、4及び5に係る発明についての無効の主張を認めるという一部無効審決をした。
本記事で紹介する判決は、特許庁がした上記審決を不服として提起された審決取消訴訟(令和2年(行ケ)10077, 10078, 10079, 10080, 10081, 10082, 10083)のうち、東和薬品が請求した特許無効審判事件の審決取消訴訟についてである。
本件訴訟(知財高裁令和2年(行ケ)10079; 10083)は、発明の名称を「5-HT1A受容体サブタイプ作動薬」とする原告(大塚製薬)の特許第4178032号について、被告(東和薬品)が特許無効審判を請求した事件(無効2018-800127号)において、特許庁が、原告の訂正を認めた上、請求項1、4及び5に係る発明についての特許を無効とし、請求項2に係る発明についての審判請求は成り立たないとする審決をしたため、原告が、本件審決のうち請求項1、4及び5に係る部分の取消しを求め(第1事件訴訟)、一方、被告が、請求項2に係る部分の取消しを求め(第2事件訴訟)た事案である。
本件発明は、エビリファイ®の有効成分であるアリピプラゾールがドーパミンD2受容体に強い親和性で結合し、ドーパミンD3受容体及び5-HT7受容体に中等度の親和性で結合すること等が報告されていたところ、5-HT1A受容体サブタイプにおける作動活性を有することを発見したことに基づき、5-HT1A受容体サブタイプに関連した中枢神経系の障害に罹患した患者を治療する方法を提供するものである。
本件明細書には5-HT1A受容体におけるアリピプラゾールの結合親和性を評価する薬理学的試験(in vitro試験)の結果が記載されていた。
本事件のポイントは、エビリファイ®(アリピプラゾール)の「うつ病・うつ状態」の効能・効果を保護する請求項2と「双極性障害における躁症状」の効能・効果を保護する請求項1、4及び5について実施可能要件・サポート要件の判断の前提となった、5-HT1A受容体部分作動薬と各疾患治療との結びつきに関する本件出願当時の技術常識の認定である。
より詳細な背景については、記事「2021.12.27 「大塚製薬 v. Meiji Seikaファルマ・大原薬品工業」 知財高裁令和2年(行ケ)10080; 10081・・・エビリファイ®用途特許一部無効審決を取り消す(判決①)」を参照。
2.要旨
Summary
- 5-HT1A部分作動薬を双極性障害の「うつ病エピソード」の治療に使用できることが技術常識であるとはいえないとした本件審決の認定に誤りがあるから、その認定を前提として本件医薬用途特許の一部が実施可能要件・サポート要件違反であるとした無効審決は取り消された。
- 但し、双極性障害の「躁病エピソード」の治療に係る部分については、本件審決において実質的な判断が示されていないとして、その部分の実施可能要件・サポート要件の適否は判断されなかった。
- 本判決に対しては、上告・上告受理申立てがされている。しかし、上告棄却・上告不受理により本判決が確定し審判が再審理となれば、その判断の帰趨は、無効審決を受けてエビリファイ®ジェネリックに「双極性障害における躁症状」の効能追加承認を与えた厚生労働省の判断と、当該効能追加販売に踏み切った各ジェネリックメーカーの決断が、それぞれ正しいものだったのかという問いに答えを与えることになるだろう。
判決の内容は以下の記事で取り上げた同日判決とほとんどの部分で重複し、結論は同じである。
参照:
- 2021.12.27 「大塚製薬 v. Meiji Seikaファルマ・大原薬品工業」 知財高裁令和2年(行ケ)10080; 10081・・・エビリファイ®用途特許一部無効審決を取り消す(判決①)
- 2021.12.27 「大塚製薬 v. ニプロ」 知財高裁令和2年(行ケ)10078; 10082・・・エビリファイ®用途特許一部無効審決を取り消す(判決②)
裁判所は、エビリファイ®の「うつ病・うつ状態」の効能・効果を保護する請求項2の無効の主張を退けた特許庁の審決を支持したが(第2事件訴訟)、「双極性障害における躁症状」の効能・効果を保護する請求項1、4及び5について無効とした審決を取り消した(第1事件訴訟)。
ここでは、被告東和薬品の主張に対する裁判所の判断の一部を紹介する。
3.薬理作用が非選択的であることは疾患とのつながりを阻害するか?
本件出願当時の5-HT1A受容体部分作動薬の抗うつ作用に関する技術常識について、「本件出願当時,5-HT1A受容体部分作動薬一般が上記5-HT1A受容体部分作動作用に基づく抗うつ作用によりうつ病に対して治療効果を有することは技術常識であったことが認められる。」と裁判所が判断したことに対して、被告は、
「選択的5-HT1A受容体作動薬ではない本件カルボスチリル化合物については,単に5-HT1A受容体作動作用により抗うつ効果があるという技術常識が存在するだけでは足りず,5-HT1A受容体作動作用に加えて,少なくとも,シナプス前ドーパミン自己受容体作動作用及びシナプス後D2受容体拮抗活性がある薬剤であっても,総合的には抗うつ効果があるという技術常識が存在する必要がある。」
等の主張をした。
しかしながら、裁判所は、以下のとおり、被告の上記主張は採用することができないと判断した。
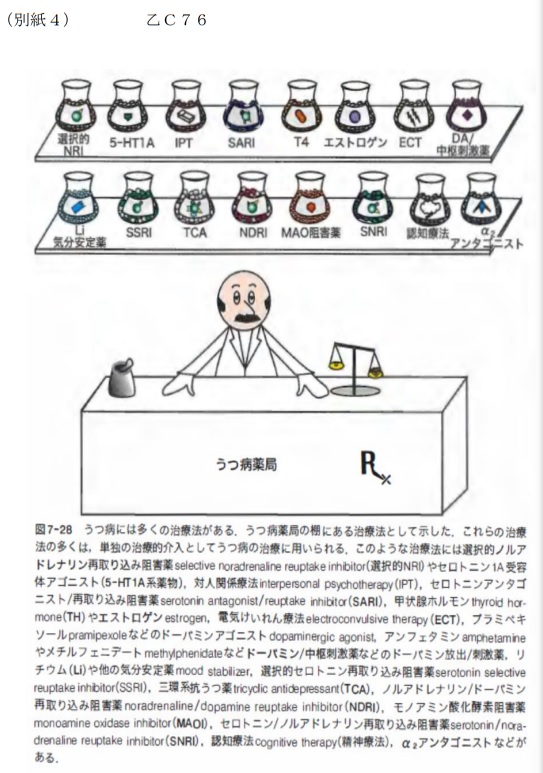
「・・・本件出願当時の精神薬理学における教科書(乙C76)や意見書・・・によれば,複
数の抗うつ薬を併用することにより,それぞれのもつ作用機序を組み合わせることが知られ,5-HT1A受容体作動薬(本件カルボスチリル化合物)についても,5-HT1A受容体以外の他の作用点によって抗うつ作用が拮抗されることなく薬理作用を発揮する(薬理作用の独立発揮性)と考えられていたこと・・・に照らすと,「選択的」,すなわち,本件カルボスチリル化合物の最も顕著な作用が5-HT1A受容体作動作用であるとは認められないことをいう・・・主張は,前記・・・認定を左右するものではない。」
薬理作用が非選択的であったとしても、非選択的であることが目的の薬理効果を発揮することに対して阻害してしまう等の特段の理由が無ければ、通常、その薬理作用を発揮するだろうと考えるのは妥当であろう。
本件及び関連事件について、その他のコメントは、以下の記事を参照。
(1)当該医薬用途発明として有用であることが技術常識といえるに足るとは
(2)知財高裁は特許庁の無効審決部分を取り消した
ア ジェネリック「うつ病・うつ状態」の効能追加承認はいつになるのか?
イ 効能・効果「双極性障害における躁症状」の攻防は続きそう
治療効果を有することを理解するにはヒト臨床試験が必須か?
>関連判決④へ

コメント