2020年2月17日、高脂血症治療剤ゼチーア®錠のジェネリック(昨年8月承認のAGを除く)の承認を取得したジェネリックメーカーは10社以上となりました。2020年6月の薬価基準収載・発売が見込まれます。ゼチーア®錠の再審査期間(2007年4月18日~2015年4月17日)が終了しているため、有効成分であるエゼチミブを保護する物質特許(第2803908号)の満了(5年の延長のため2019年9月14日)以降、早ければ2020年2月にジェネリックが承認されると推測されていました。
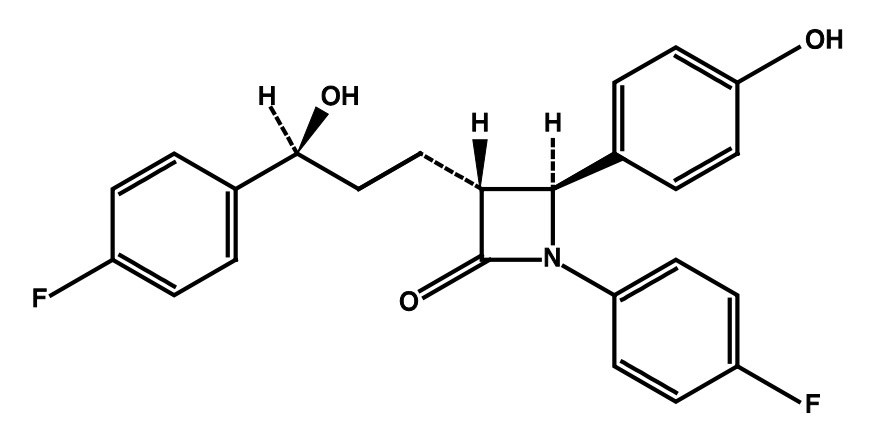
ゼチーア®錠は、米国シェリング・プラウ社(現 Merck Sharp & Dohme Corp., a subsidiary of Merck & Co.,Inc.)により創製された世界初の小腸コレステロールトランスポーター阻害剤である高脂血症治療剤(有効成分: エゼチミブ(Ezetimibe))。日本ではMSD/バイエル薬品が販売していますが、第一三共エスファが2019年8月にオーソライズド・ジェネリック(AG)であるエゼチミブ錠 10mg「DSEP」の承認を取得し、発売開始を2020年6月に予定していると発表しています。従って、AGと他のジェネリックとが横並びで同時期に一斉に発売になると思われます。
- 2020.02.03 第一三共エスファ press release: 発売予定製品のご案内
ゼチーア®錠およびAGの効能・効果は「高コレステロール血症、家族性高コレステロール血症、ホモ接合体性シトステロール血症」であるのに対し、他のジェネリックの効能・効果は「高コレステロール血症、家族性高コレステロール血症」のみとなっています。「ホモ接合体性シトステロール血症」については用途特許(第4614460号および第4711600号)が存続しているため(2022年1月25日満了)、パテントリンケージによりジェネリックは効能効果の虫食い承認となったと思われます。


コメント
エゼチミブDSEPとゼチーアの違いを知りたい。いままでずっとゼチーアを使用してきたがジェネリックはいろんな違いがあって、できれば使用しない方が良いと知り合いの医師に聞いた。同じ会社でなぜジェネリック薬品を出すのか?なぜ安くできるのか?先発品のゼチーアが売れなくなるのではないか?二つの薬の成分、添加物に違いはあるのか?疑問だらけです。
コメントありがとうございました。
・先発医薬品を保護する特許が満了すれば、後発医薬品メーカーは、先発メーカーのような多大な開発費を投入しなくても(開発失敗のリスクもなく)ジェネリック(後発医薬品)を申請・承認・販売が可能になりますので、先発品より安価なジェネリックでも事業が成り立ち得ます(薬価は先発品より安価に設定される)。従って、先発医薬品はそれまで独占していたシェアを安価なジェネリックに奪われることになります。
・ジェネリックは先発医薬品と有効成分が同じで生物学的同等性が認められたものですが、添加物が同一とは限りません。しかし、エゼチミブ錠「DSEP」は、MSD社が製造販売しているゼチーア®錠と原薬、添加物及び製造方法・製造場所が、それぞれ同一のオーソライズド・ジェネリックですので、実質ゼチーア®錠と同じものといえます。
・先発メーカーは、特許が満了して多くのジェネリックにより市場を奪われるくらいなら、他社(子会社の場合もあり)と提携してオーソライズド・ジェネリックを投入して安価であってもジェネリックの中でシェアを維持しようとする戦略をとる場合があります。
2022.01.25 高脂血症治療剤ゼチーア®(有効成分エゼチミブ)の「ホモ接合体性シトステロール血症」についての用途特許満了日。
2022.01.26 「高コレステロール血症、家族性高コレステロール血症」に限られていたゼチーア®ジェネリックの各社が「ホモ接合体性シトステロール血症」についての効能・効果追加承認取得を発表。先発品ゼチーア®と効能効果が同じとなる。少なくとも以下各社のニュースあり。