そう痒症改善剤ノピコール®の特許権の存続期間の延長登録無効審決の取消し・・・「ナルフラフィン塩酸塩」のみを本件医薬品の有効成分と解し、「ナルフラフィン」は本件医薬品の有効成分ではないと認定して、本件発明の実施に本件処分を受けることが必要であったとはいえないと判断した本件審決の認定判断は誤り
1.はじめに
本件(知財高裁令和2年(行ケ)10096)は、東レが保有する「止痒剤」に関する特許権の存続期間の延長登録(出願番号2015-700061)を無効とする審決(無効2020-800002号)に対する取消訴訟である。
争点は、①被告ニプロに被告適格があるか否か、②本件特許(第3531170号)を実施するために本件処分を受けることが必要であったか否かである。
なお、上記①については、被告ニプロに被告適格があり、被告ニプロの被告適格に対する本案前の抗弁は理由がないとする中間判決が言い渡されている(2020.12.02 「東レ v. 沢井製薬・ニプロ」 知財高裁令和2年(行ケ)10096, 令和2年(行ケ)10097, 令和2年(行ケ)10098(中間判決))。
裁判所は、上記②について、本件審決の認定判断は誤りであり、原告が主張する取消事由1(本件医薬品の有効成分に関する事実認定の誤り)は理由があるとして、審決を取消した。
本事件と判決内容は「2021.03.25 「東レ v. 特許庁長官」 知財高裁令和2年(行ケ)10063」と共通する部分が多いのでそちらも参照。
2.経緯
(1)本件特許(第3531170号)
【発明の名称】止痒剤
【特許番号】特許第3531170号
【登録日】2004.03.12
【出願番号】特願平10-524506
【出願日】1997.11.21
【優先日】1996.11.25
【特許権者】東レ株式会社
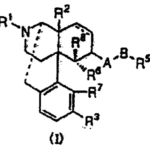
【請求項1】下記一般式(I)
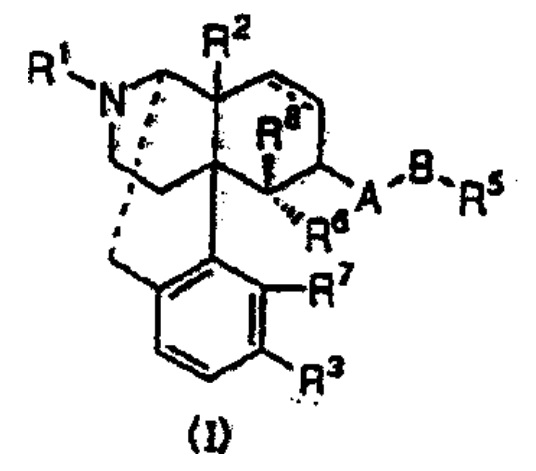
[式中、・・・(省略)・・・]で表されるオピオイドκ受容体作動性化合物を有効成分とする止痒剤。
(2)本件処分
本件延長登録は、以下の処分に基づくものである。
イ 延長登録の理由となる処分
医薬品,医療機器等の品質,有効性及び安全性の確保等に関する法律(以下「薬機法」という。)14条1項に規定する医薬品に係る同項の承認
ウ 処分を特定する番号 22600AMX01388000
エ 処分を受けた日 平成26年12月26日
オ 処分の対象となった医薬品
販売名 ノピコールカプセル2.5μg
有効成分 ナルフラフィン塩酸塩
カ 処分の対象となった医薬品について特定された用途
慢性肝疾患患者におけるそう痒症の改善(既存治療で効果不十分な場合に限る)
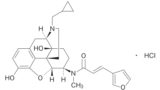
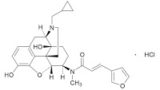
本件医薬品は、経口そう痒症改善剤「ノピコール®カプセル2.5μg」(一般名:ナルフラフィン塩酸塩)であるが現在販売中止。同一成分薬として「レミッチ®カプセル 2.5μg」がある。
- 2015.05.26 東レ・メディカル(株)・(株)オーファンパシフィック press release: 経口そう痒症改善剤「ノピコール®カプセル2.5μg」の発売について
(3)本件審決
被告沢井製薬は本件延長登録について無効審判(無効2020-80002号事件)を請求し(被告ニプロは参加)、特許庁は、「特許第3531170号の特許権存続期間延長登録出願2015-700061号に基づく特許権の存続期間の延長登録を無効とする。」との審決をした。
3.取消事由1(本件医薬品の有効成分に関する事実認定の誤り)について
(1)原告の主張
ア 本件審決の事実認定の誤り
本件医薬品は,本件発明1の「一般式(Ⅰ)で表されるオピオイドκ受容体作動性化合物」であるナルフラフィン(フリー体)を有効成分とする医薬品であり,本件発明1の発明特定事項を備えているものであるが,本件審決は,本件医薬品の有効成分がナルフラフィン塩酸塩であると誤って認定している。
以下で詳述するとおり,医薬品の有効成分に関する技術常識,ナルフラフィン塩酸塩の有効成分に関する科学的・客観的な理解,本件医薬品の製造販売承認書(以下「本件承認書」という。)の記載等からすると,本件医薬品がナルフラフィンを有効成分とする止痒剤であることは明らかである。
イ 被告らの主張に対する反論
本件発明が医薬用途発明であることを踏まえて本件発明との関係で本件医薬品を特定すると,注目されるべきは当該用途(止痒)に係る作用効果を奏する成分が何であるかであって,医薬品中に含有される有効成分の存在形態は問題となり得ず,当業者は,本件医薬品の「有効成分」を止痒効果を奏する成分であるナルフラフィン(フリー体)であると一義的に理解する。
被告らは,医薬品としての安定性,生体内における溶解性に差異があると,その薬効にも影響があるなどと主張する。
しかし,本件発明は有効成分となる化合物について止痒剤としての新たな医薬用途を見いだした医薬用途発明であり,被告らの主張は,本件発明の性質等を無視したもので失当である。
(2)被告らの主張
「ナルフラフィン塩酸塩」を有効成分とする本件医薬品は・・・「ナルフラフィン」を有効成分とする本件発明1の発明特定事項を・・・備えていないから,本件発明の実施に本件処分を受けることが必要であったとは認められない。
本件処分の対象となった本件医薬品は,本件延長登録出願や本件延長登録,本件インタビューフォーム(甲9)及び本件添付文書(甲11)においても,一貫して「ナルフラフィン塩酸塩」を有効成分としていることが明白であり,実際の「止痒剤」(そう痒症の改善)を用途とする本件医薬品もナルフラフィン塩酸塩である。
原告が提出した証拠に記載された「有効成分」との用語の意義は,いずれも医薬品をヒトに投与した後,「生体内」において薬効を生じる時点における成分を意味するものであり,「医薬品」として製造され,販売される場合における成分を意味するものではない。
一般に医薬品の特許発明の実施において問題とされるべきものは,「物」としての医薬品が製造され,販売される場合における有効成分の存在形態である。それは,医薬品の医薬品製造販売承認書において「成分名」として記載されている。その医薬品がヒトに投与され,生体内においてどのような存在形態をとるかが問題となるわけではない。
4.裁判所の判断(抜粋)
主 文
1 特許庁が無効2020-800002号事件について令和2年7月28日にした審決を取り消す。
2 訴訟費用は被告らの負担とする。
(1)本件発明の実施に本件処分を受けることが必要であったかどうかについて検討
ア 特許権の存続期間の延長登録の制度は,政令処分を受けることが必要であったために特許発明の実施をすることができなかった期間を回復することを目的とするものであるから,本件発明の実施に本件処分を受けることが必要であったかどうかは,このような特許法の存続期間延長の制度が設けられている趣旨に照らして判断されるべきであり,その場合における本件処分の内容の認定についても,このような観点から実質的に判断されるべきであって,承認書の「有効成分」の記載内容から形式的に判断すべきではない。このように解することは,最高裁平成26年(行ヒ)第356号同27年11月17日第三小法廷判決・民集69巻7号1912頁の趣旨にも沿うものということができる。
イ 前記(1)エで認定した事実からすると,医薬品について,良好な物性と安定性の観点からフリー体に酸等が付加されて,フリー体とは異なる化合物(付加塩)が医薬品とされる場合があること,そのような医薬品が人体に取り込まれたときには,付加塩からフリー体が解離し,フリー体が薬効及び薬理作用を奏すること,ナルフラフィンとナルフラフィン塩酸塩についても同様の関係にあり,ナルフラフィンとナルフラフィン塩酸塩で薬効及び薬理作用に違いがないことは,平成25年10月25日に本件医薬品の製造販売の承認申請がされた時までに,当業者に広く知られていたものと認められる。
ウ 上記イで述べたところに,前記(1)オ,カ,キで認定した事実や前記(1)クの専門家の意見書の内容を総合すると,医薬品分野の当業者は,医薬品の目的たる効能,効果を生ぜしめる作用に着目して,付加塩だけでなく,そのフリー体も「有効成分」と捉えることがあるものと認められる。
エ 前記(1)ア~ウのとおり,本件承認書には,「成分」として「ナルフラフィン塩酸塩」と記載されていて,本件添付文書にも「有効成分に関する理化学的知見」として,「ナルフラフィン塩酸塩」と記載され,その構造式や性状などが記載されているが,これは,賦形剤などの製剤補助剤と区別する観点から,実際に医薬品に配合されている原薬(付加塩)を有効成分として捉えていることに基づく記載であると解される。これに対し,本件添付文書の「有効成分・含量(1カプセル中)」の欄に,「ナルフラフィン塩酸塩2.5μg(ナルフラフィンとして2.32μg)」と記載されており,本件インタビューフォームには,和名は「ナルフラフィン塩酸塩」と記載されているものの,洋名については「ナルフラフィン塩酸塩」と「ナルフラフィン」が併記されているし,「有効成分(活性成分)の含量」として,「1カプセル中ナルフラフィン塩酸塩2.5μg(ナルフラフィンとして2.32μg)含有」と記載されている。そして,前記(1)アのとおり,本件承認書では,・・・同じく,前記(1)イ,ウのとおり,本件添付文書や本件インタビューフォームにおける,本件医薬品の「薬物動態」の血漿中濃度推移や薬物動態パラメータもナルフラフィン塩酸塩ではなく,ナルフラフィンを測定して得られたものとなっている。
オ 以上のことを考え併せると,本件処分の対象となった本件医薬品の有効成分は,本件承認書に記載された「ナルフラフィン塩酸塩」と形式的に決するのではなく,実質的には,本件医薬品の承認審査において,効能,効果を生ぜしめる成分として着目されていたフリー体の「ナルフラフィン」と,本件医薬品に配合されている,その原薬形態の「ナルフラフィン塩酸塩」の双方であると認めるのが相当である。
したがって,「ナルフラフィン塩酸塩」のみを本件医薬品の有効成分と解し,「ナルフラフィン」は,本件医薬品の有効成分ではないと認定して,本件発明の実施に本件処分を受けることが必要であったとはいえないと判断した本件審決の認定判断は誤りであり,取消事由1は理由がある。
(2)被告らの主張について
①ナルフラフィン塩酸塩が有効成分の一般的名称(JAN)とされていること、について
本件医薬品の「一般名」のうち,「和名」はナルフラフィン塩酸塩であるが,他方で,「洋名」のうち,国際一般的名称(INN)は,「nalfurafine」であるから,「一般名」のみで有効成分を特定することができるというものではなく,被告沢井製薬の主張するところが,前記(2)の認定判断を左右するものとはいえない。
②医薬品にとって溶解性等はその作用効果として重要であるから、酸付加塩の有無は、投与時における有効成分として理解されるべきであること、及び③本件特許との関係では、生体内における存在形態ではなく、販売される場合の有効成分の存在形態が問題とされるべきであること、について
溶解性や安定性の向上などのために,本件医薬品の原薬形態が,ナルフラフィン塩酸塩とされていることは,前記(1)エ(エ)で認定したとおりであるが,前記(1)で認定した事実からすると,前記(2)で認定判断したとおり,投与時の原薬形態であるナルフラフィン塩酸塩のみならず,本件医薬品の承認審査で,効能,効果を生ぜしめる成分として着目されていた,ヒトに投与した後の形態であるフリー体のナルフラフィンも,本件医薬品の「有効成分」と認定することができる。
前記2で認定したように,本件発明は,一般式(I)で示される化合物をはじめとする特定のオピオイドκ受容体作動性化合物を有効成分とした止痒剤に関する発明であり,本件発明の技術的意義が,販売される場合のオピオイドκ受容体作動性化合物の存在形態にあるものとは認められないから,そのような販売される場合の存在形態の違いによって,本件処分における本件医薬品の有効成分の認定が左右されるとは解されない。
④「フリー体と酸付加塩の両方で承認取得した事例」や「フリー体と酸付加塩で効能効果が違う事例」が存在することについて
薬機法上,医薬品の製造販売承認において,フリー体と酸付加塩で異なる承認が得られる場合があったとしても(乙1~4),本件医薬品の処分の内容は,特許法において存続期間の延長登録制度が設けられている趣旨に照らし,特許法の観点から実質的に,認定判断されるべきものであるから,それらの事例の存在が,本件処分の内容を前記(2)のように認定することを妨げるものということはできない。
(3)結論
以上の次第で,取消事由1は理由がある。よって,その余の点について判断するまでもなく,本件審決にはその結論に影響を及ぼす違法があるから,原告の請求を認容することとして,主文のとおり判決する。
5.コメント
(1)本件発明の実施に本件処分を受けることが必要であったかどうかは実質的に判断すべき
本件特許の請求の範囲は「ナルフラフィン」のフリー体を保護するもので、本件医薬品に配合されている原薬形態の「ナルフラフィン塩酸塩」を範囲に含まないようである。この点、特許庁は、本件医薬品の有効成分は「ナルフラフィン塩酸塩」であるとして本件延長登録を無効であると審決した。
しかし、知財高裁は、特許権の存続期間延長制度の趣旨に照らして、実質的に登録可否を判断すべきであるとの一般原則を示したうえで、本件においては、実質的には、効能・効果を生ぜしめる成分はフリー体の「ナルフラフィン」であるから、「ナルフラフィン」も本件医薬品の有効成分であると認め、従って、本件発明(「ナルフラフィン」のフリー体)の実施に本件処分を受けることが必要であった、ということを判断したといえる。
本件発明の実施に本件処分を受けることが必要であったかどうかは,このような特許法の存続期間延長の制度が設けられている趣旨に照らして判断されるべきであり,その場合における本件処分の内容の認定についても,このような観点から実質的に判断されるべきであって,承認書の「有効成分」の記載内容から形式的に判断すべきではない。このように解することは,最高裁平成26年(行ヒ)第356号同27年11月17日第三小法廷判決・民集69巻7号1912頁の趣旨にも沿うものということができる。
この「実質的に判断されるべきで、形式的に判断すべきではない」という観点は、場面は異なるが、先行処分との関係で「効能・効果」の異同が争点となった過去判決でも同様の言及が見られる(本件裁判所が引用した最高裁平成26年(行ヒ)第356号含む)。本件は「有効成分」の解釈が問題となった事例ではあるが、承認書等の記載から「実質的に判断されるべきで、形式的に判断すべきではない」という点は、延長登録の可否を判断するうえで共通する大原則といえよう。
過去判決につていは、記事「2021.03.25 「東レ v. 特許庁長官」 知財高裁令和2年(行ケ)10063」にて引用している。

(2)「フリー体の特許発明を実施する」ことの意味
「ナルフラフィン」は本件医薬品の有効成分ではないと認定して本件発明の実施に本件処分を受けることが必要であったとはいえないとした本件審決の認定は誤りであると判断した知財高裁。
すなわち、本件発明であるフリー体の実施に本件処分を受けることが必要であったことを認めた判断といえる。
物の発明について、「実施」とは・・・。
様々な論点・議論を生み出しそうだ。
(3)ノピコール®の延長特許権の効力はレミッチ®のジェネリックに及ぶのか
本件医薬品は、経口そう痒症改善剤「ノピコール®カプセル2.5μg」(一般名:ナルフラフィン塩酸塩)であるが現在販売は中止されている。
「ノピコール®カプセル2.5μg」の慢性肝疾患患者におけるそう痒症の改善についての効能・効果の承認に基づいて延長された特許権の効力は、形式的には、処分の対象となった物(「ノピコール®カプセル2.5μg」)以外には及ばないはずだが、同一成分薬として「レミッチ®カプセル 2.5μg」があり、実質的には、同効能・効果を標榜するレミッチ®カプセルのジェネリックにもその効力は及ぶと考えられる。
(4)別件審決取消訴訟
本件特許に係る特許権は、東レが製造販売する経口そう痒症改善剤レミッチ®(一般名: ナルフラフィン塩酸塩)を保護し、その20年の存続期間満了日は2017年11月21日だが、期間延長出願(特願2015-700061(本件延長登録)、特願2017-700154、特願2017-700309、特願2017-700310)により現在も存続している。
本件特許については、無効審判請求不成立審決取消訴訟(記事参照:2021.03.25 「沢井製薬 v. 東レ」 知財高裁令和2年(行ケ)10041)、延長登録出願拒絶審決取消訴訟(記事参照:2021.03.25 「東レ v. 特許庁長官」 知財高裁令和2年(行ケ)10063)、及び本件含む期間延長登録の無効審決取消訴訟(以下の3件)の各判決が同日に言い渡されている(いずれも無効審決の取消し。残り2件については後日ブログで取り上げる予定)。
- 令和2年(行ケ)10096:特許3531170号の下記処分(承認)に基づく延長登録(2015-700061)の無効審決(無効2020-800002号事件)取消訴訟(本件)。
(1)処分の対象となった医薬品
販売名 ノピコールカプセル2.5μg
有効成分 ナルフラフィン塩酸塩
(2)処分の対象となった医薬品について特定された用途
慢性肝疾患患者におけるそう痒症の改善(既存治療で効果不十分な場合に限る)
- 令和2年(行ケ)10097:特許3531170号の下記処分(承認)に基づく延長登録(2017-700309)の無効審決(無効2020-800003号事件)取消訴訟。
(1)処分の対象となった医薬品
販売名 レミッチカプセル2.5μg
有効成分 ナルフラフィン塩酸塩
(2)処分の対象となった医薬品について特定された用途
次の患者におけるそう痒症の改善(既存治療で効果不十分な場合に限る)
透析患者(血液透析患者を除く)、慢性肝疾患患者
- 令和2年(行ケ)10098:特許3531170号の下記処分(承認)に基づく延長登録(2017-700310)の無効審決(無効2020-800004号事件)取消訴訟。
(1)処分の対象となった医薬品
販売名 レミッチOD錠2.5μg
有効成分 ナルフラフィン塩酸塩
(2)処分の対象となった医薬品について特定された用途
次の患者におけるそう痒症の改善(既存治療で効果不十分な場合に限る)
透析患者(血液透析患者を除く)、慢性肝疾患患者
6.おわりに
2018年6月よりレミッチ®の後発医薬品である「ナルフラフィン塩酸塩OD錠2.5μg「サワイ」」の製造販売を開始した沢井製薬に対して東レは特許権侵害訴訟を提起している(下記過去記事参照)。
- 2019.10.20 レミッチ®用途特許に対するジェネリックメーカーの動き
- 2018.12.12 東レがレミッチ®OD錠後発品を販売する沢井・扶桑を特許侵害で提訴

すなわち延長された特許権(医薬用途発明)の行使を争う事件であり、まだ判決例の少ない延長された特許権の効力についての裁判所による判断がどうなるのか注目される。
本件特許について無効審判請求不成立審決取消訴訟で東レが勝訴(記事参照:2021.03.25 「沢井製薬 v. 東レ」 知財高裁令和2年(行ケ)10041)、延長登録出願拒絶審決取消訴訟で東レが勝訴(記事参照:2021.03.25 「東レ v. 特許庁長官」 知財高裁令和2年(行ケ)10063)、そして、本件でも知財高裁が本件延長登録の無効審決を取消し、東レが勝訴したことで、侵害訴訟の行方は大きな影響を受けると思われる。

コメント