1.謹告「ゾレドロン酸に関する特許権について」の再掲載
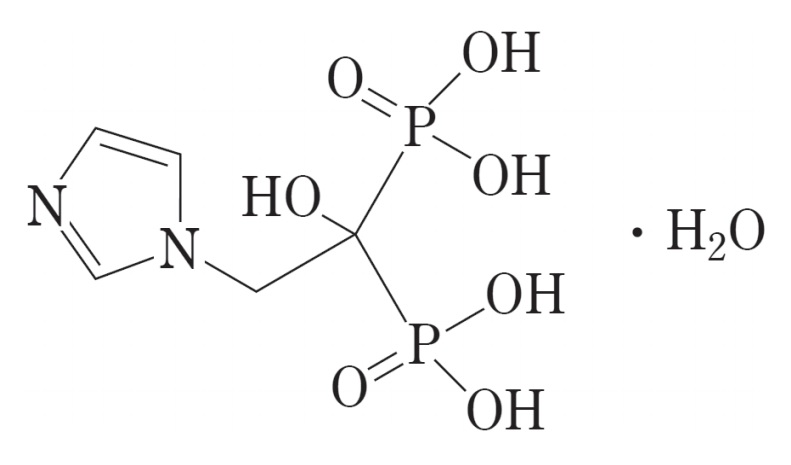 2022年1月28日、ノバルティスファーマおよび旭化成ファーマより「ゾレドロン酸に関する特許権について」の謹告文が掲載されました(参考: 2022.01.28 日刊薬業 【謹告】ゾレドロン酸に関する特許権について)。
2022年1月28日、ノバルティスファーマおよび旭化成ファーマより「ゾレドロン酸に関する特許権について」の謹告文が掲載されました(参考: 2022.01.28 日刊薬業 【謹告】ゾレドロン酸に関する特許権について)。
謹告文によると、ノバルティスファーマは、ビスホスホネートの投与法に関する特許権(日本特許第4722375号、日本特許第5005188号)、およびビスホスホネートを含む医薬製品に関する特許権(日本特許第4802096号)を保有しており、旭化成ファーマは、これら特許権の専用実施権者として、ゾレドロン酸を有効成分とする骨粗鬆症治療剤「リクラスト®点滴静注液5mg」を製造販売しています。
ノバルティスファーマおよび旭化成ファーマは、両社の特許権および専用実施権を侵害する行為、または侵害するおそれのある行為に対して、厳正なる法的処置を講じるとのことです。
既に2020年9月25日にも同様の謹告文が掲載されています。
- 記事参照: 2020.09.26 骨粗鬆症治療剤(ビスホスホネート製剤)「リクラスト®点滴静注液5mg」・・・ゾレドロン酸に関する特許権について)
2.「リクラスト®点滴静注液 5mg」に関する特許権について
前回の謹告文が掲載された際の記事(2020.09.26 骨粗鬆症治療剤(ビスホスホネート製剤)「リクラスト®点滴静注液5mg」・・・ゾレドロン酸に関する特許権について)にて取り上げた特許権の現在の状況を以下にアップデートしました(再審査期間が終了した以外に前回からの変更はありません)。
| リクラスト®点滴静注液 5mg | ・効能又は効果・・・骨粗鬆症。 ・用法及び用量・・・通常、成人には1年に1回ゾレドロン酸として5mgを15分以上かけて点滴静脈内投与する。 ・製剤の組成及び物性・・・1 ボトル100mL中ゾレドロン酸水和物5.33mg(ゾレドロン酸として5.0mg)、添加剤として、D-マンニトール、クエン酸ナトリウム水和物、注射用水。pH: 6.0 ~ 7.0。 ・容器の材質・・・プラスチックボトル(無色):シクロオレフィンポリマー。 | 再審査期間4年 (2016.09.28~2020.09.27) |
| 特許第4722375号 | 【請求項1】 間歇的に投与され、かつ、投与の間隔が少なくとも1年であり、さらに静脈内投与される、骨粗鬆症の処置用医薬であって、有効成分として1-ヒドロキシ-2-(イミダゾール-1-イル)エタン-1,1-ジホスホン酸またはその薬学的に許容される塩もしくは水和物を単位投与量として1~10mg含有する医薬。 | 特許権存続期間満了日 2026.06.18 |
| 特許第5005188号 | 【請求項1】 ゾレドロン酸またはその薬学的に許容される塩、またはその水和物を単位投与量として1~10mg含有する骨粗鬆症の処置用医薬であって、間歇的に静脈内投与され、かつ、投与の間隔が少なくとも6ヶ月である医薬。 | 特許権存続期間満了日 2025.10.14 |
| 特許第4802096号 | 【請求項1】 すぐに使用できる溶液の形態の医薬製品であって、 ゾレドロン酸または薬理学的に許容されるその塩の溶液を含有する容器を含み、 該容器の少なくとも内側表面はシクロオレフィンポリマーであるプラスチック材を含み、 該充填された容器は加熱滅菌可能であり、 該溶液は、さらに有機塩基性緩衝剤を含み、そして、生理学的に許容されるpH値であるpH5.5~8.0に該有機塩基を用いて調整されたものであり、 該製品は100mlの量を有する単位用量形態であり、 該単位用量形態は4~5mgの無水ゾレドロン酸と等価の量のゾレドロン酸または薬理学的に許容されるその塩を含む、 医薬製品。 | 特許権存続期間満了日 2029.09.17 |
リクラスト®点滴静注液 5mgの再審査期間は2020年9月に終了したことから、ジェネリックの承認申請がされている可能性があります。
しかし、ビスホスホネートの投与法に関する特許権として挙げられている特許第4722375号及び特許第5005188号は、リクラスト®点滴静注液 5mgの用法及び用量を保護するものであり、有効に存続しています。
リクラスト®点滴静注液 5mgのジェネリックは用法及び用量を別の構成に変えて承認を得ることは困難であることから、用法及び用量についてのこれら特許が有効に存在する限り、パテントリンケージにより、リクラスト®点滴静注液 5mgと同じ用法・用量となるジェネリックは承認されないと考えられます(*1)。
したがって、リクラスト®点滴静注液 5mgのジェネリックの承認取得を目指しているジェネリックメーカーは、これら特許の無効審判を請求して特許無効審決を勝ち取らない限り、特許権が満了(2026年6月18日)する前にジェネリックの承認は取得できないと思われます。
現時点で、上記3つの特許に対して無効審判は請求されていないため、リクラスト®点滴静注液 5mgのジェネリックを参入しようと目論むジェネリックメーカーがいるのかは不明(*2)ですが、ノバルティスファーマ及び旭化成ファーマは、この再審査期間終了のタイミングでジェネリックの承認取得を計画しているジェネリックメーカーに対して謹告文を掲載することにより牽制したいと考えたようです。
特許第4802096号の特許請求の範囲は、容器の内側表面をシクロオレフィンポリマーに限定するものです。ジェネリックメーカーが、シクロオレフィンポリマー以外の材質を容器に採用できれば、この特許権による権利行使から免れることができそうです。
ーーー
(*1) 「医療用後発医薬品の薬事法上の承認審査及び薬価収載に係る医薬品特許の取扱いについて(各都道府県衛生主管部(局)長あて厚生労働省医政局経済課長・厚生労働省医薬食品局審査管理課長通知)(平成21年6月5日付医政経発第0605001号/薬食審査発第0605014号)」及び「承認審査に係る医薬品特許情報の取扱いについて(平成6年10月4日付け薬審第762号審査課長通知)」において、後発医薬品の薬事法上の承認審査にあたっては、
- 先発医薬品の有効成分に特許が存在する場合には後発医薬品を承認しないこと
- 先発医薬品の特許が存在する効能・効果、用法・用量(効能・効果等)については承認しない方針であること
- 特許の存否は承認予定日で判断するものであること
を定めています。日本版パテントリンケージについては2021.03.08記事「日本のパテントリンケージの現状の課題とその解決に向けた提案」をご参照ください。
(*2) 旭化成(株)決算説明会資料によると、旭化成ファーマ(株)によるリクラスト®の国内売上は、発売2016年度4億円→2017年度11億円→2018年度14億円→2019年度14億円→2020年度13億円と推移している。多くの骨粗鬆症治療薬がある中でのビスホスホネート製剤、さらにその中でも月1回投与製剤がある中での年1回の点滴静注という特徴が製品価値としてどれだけ高く市場で評価されているのか、その売上の伸びを見ると・・・?である。ジェネリックメーカーにとってリクラスト®のジェネリック参入の魅力度は高いのだろうか。リクラスト®については、旭化成ファーマのリクラスト®を紹介するウェブサイト「リクラスト®情報局」参照。

コメント