特許発明の技術的範囲を明細書記載から限定解釈: 東京地裁平成26年(ワ)25013
【背景】
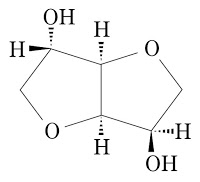
「メニエール病治療薬」に関する特許権(第4778108号)を有する原告(X)が、被告ら(興和及び興和創薬)による被告製品イソバイドシロップ(有効成分: イソソルビド(Isosorbide))の製造販売が上記特許権の侵害に当たると主張して、被告製品製造等差止め及び損害賠償を求めた事案。
本件発明は次の構成要件に分説される。
A 成人1日あたり0.15~0.75g/kg体重のイソソルビトールを経口投与されるように用いられる(以下「構成要件A」という。)
B (ただし,イソソルビトールに対し1~30質量%の多糖類を,併せて経口投与する場合を除く)ことを特徴とする,
C イソソルビトールを含有するメニエール病治療薬。
【要旨】
主文
原告の請求をいずれも棄却する。(他略)
裁判所の判断
争点(1)(被告製品における構成要件Aの充足性)について
原告は、
「被告製品はいずれも患者の体重及び投与量が一定の範囲内にある場合には「成人1日あたり0.15~0.75g/kg体重のイソソルビトールを経口投与されるように用いられる」ものとなるので,構成要件Aを充足する」
と主張した。
しかし、裁判所は、本件明細書の発明の詳細な説明の欄には次の趣旨の記載
「 (3) ア(オ)発明の効果(段落【0032】)
薬剤の投与量は,個人差,病状の重篤度などに合わせて適宜調節されなくてはならず,投与量を削減しても,同等又は同等以上の効果が得られることは臨床で頻繁に遭遇することである。しかし,本発明で投与量を削減する意味は,そのようないわゆる「医師のさじ加減」とは異なる。本発明の本質は,投与薬剤量が従来のままでは治療効果が十分には発現せず,投与量を削減して初めて治療効果が確実に増強することを発見し,証明したことで,大量投与による様々な問題を一挙に解決する治療薬を開発したことにある。」
等があることを踏まえ、下記のとおり判断した。
「~本件明細書の記載によれば,本件発明は,従来のイソソルビトール製剤(これが被告製品1を指すことは明らかであり,その標準用量は1日当たりイソソルビトール1.05~1.4g/kg体重に相当する。甲3)の投与量が過大であり,そのために種々の問題が生じるところ,その投与量を構成要件Aに記載の0.15~0.75g/kg体重という範囲にまで削減することによって上記の問題を解消したというものである。そうすると,本件発明の治療薬は,構成要件A記載の範囲を超える量のイソソルビトールを投与する用法を排除し,従来より少ない量を投与するように用いられる治療薬に限定されるということができる。換言すると,上記範囲を超える量のイソソルビトールを投与するように用いられる治療薬は,「医師のさじ加減」個々の患者の特徴や病態の変化に応じて医師の判断により投与量が削減された場合には構成要件Aに記載された量で用いられ得るものであっても,本件発明の技術的範囲に属しないと解すべきである。このことは~実施例又は参考例において,イソソルビトールの投与量を時間的推移に着目して変動させたものが見当たらないことからも裏付けられると解される。
したがって,構成要件Aの「成人1日あたり0.15~0.75g/kg体重のイソソルビトールを経口投与されるように用いられる」とは,上記の用量を,患者の病態変化その他の個別の事情に着目した医師の判断による変動をしない段階,すなわち治療開始当初から,患者の個人差や病状の重篤度に関わりなく用いられることをいうものと解するのが相当である。
以上の解釈に基づき,被告製品が構成要件Aを充足するか否かについてみるに,一般に,薬剤の用法用量は添付文書に記載され(医薬品,医療機器等の品質,有効性及び安全性の確保等に関する法律52条1項1号),医薬品の製造販売業者から提供される(同法68条の2第1項)ことが義務づけられていることに照らすと,被告製品が構成要件Aを充足するというためには,構成要件A所定の用法用量が添付文書に記載されていること又は製造販売業者が提供する情報に含まれていることが必要であると考えられる。
ところが~被告製品の添付文書,インタビューフォーム及びくすりのしおりに記載された用量に構成要件A所定の用量は含まれていない。なお,上記添付文書等には「症状により適宜増減する」という記載があるが,ここにいう適宜増減とは,投与開始時の患者の病状やその後の変化を踏まえ,医師の判断により投与量を増減させることをいうと解されるから,適宜増減の結果イソソルビトールの投与量が構成要件A所定の範囲に含まれる場合があるとしても,これをもって被告製品が本件発明の技術的範囲に属するということはできない。
また,本件ウェブサイトは,医師に対する情報提供の趣旨を含んでいると解されるが,投与量の漸減について記載したものであって,投与開始時における用量には構成要件A所定の用量が含まれていない。
したがって,被告製品が構成要件Aを充足するということはできない。」
【コメント】
特許発明の技術的範囲が明細書の記載から限定解釈された事例である。
また、特許発明の技術的範囲の限定的解釈に基づき、被告製品が構成要件Aを充足するか否かについては、被告製品の添付文書に記載されていること又は製造販売業者が提供する情報に含まれていることが必要であると裁判所は考えた。結論としては、医師の判断による投与量の増減は構成要件Aを充足しないと判断した。
本件特許のファミリー状況(欧米には出願していない):
- 特願2010-255729、特願2008-231796の分割、特開2011-032288、特許4778108(本件特許)
- 特願 2011-097047、特願2010-255729の分割、特開2011-148825、特許4865924
請求項1:
成人1日あたり0.15~0.75g/kg体重のエリスリトールを経口投与されるように用いられる(ただし、エリスリトールに対し1~30質量%の多糖類を、併せて経口投与する場合を除く)ことを特徴とする、エリスリトールを含有するメニエール病治療薬。 - 特願2008-231796、特開2009-256308、特許4676522
請求項1:
糖アルコールを含有するメニエール病治療薬において、糖アルコールがエリスリトールで、1投与単位当たり3~10g含有するように製剤化したことを特徴とするメニエール病治療薬。請求項2:
糖アルコールを含有するメニエール病治療薬において、糖アルコールがイソソルビトールで、1投与単位当たり3~10g含有するように製剤化したことを特徴とするメニエール病治療薬。 - 特願2008-185628、特開2009-256303、特許4385343
請求項1(他略):
グリセロール、エリスリトール、キシリトール、キシロース、ソルビトール、イソソルビトール、及びマンニトールよりなる群から選ばれる2種以上の単糖類又はその糖アルコールを含有するメニエール病治療薬。
イソバイドシロップ(イソソルビド(Isosorbide))のインタビューフォームによれば、イソソルビドは米国において1965年に承認され、本邦においては販売名「イソバイド」が利尿作用、脳圧降下作用及び眼圧降下作用を適応とする浸透圧利尿薬として、1968年4月に承認されていたが、その後、1980 年代にメニエール病に対するイソソルビド(イソバイド)の治療効果に関する報告が発表され、各種臨床試験により有効性が確認されたことより、1988年2月にメニエール病治療薬として適応が認められた。また、製剤の組成または用法用量は下記のとおりとなっている。
製剤の組成:
(1)有効成分(活性成分)の含量
- イソバイドシロップ70% :500mL 中イソソルビドを350.0g 含有
- イソバイドシロップ70%分包20mL :20mL 中イソソルビドを14.0g 含有
- イソバイドシロップ70%分包23mL :23mL 中イソソルビドを16.1g 含有
- イソバイドシロップ70%分包30mL :30mL 中イソソルビドを21.0g 含有
(2)添加物
- 乳酸、D-ソルビトール、サッカリンNa、パラベン、香料
用法および用量:
- メニエール病の場合には、1 日体重当り1.5~2.0mL/kg を標準用量とし、通常成人1 日量90~120mL を毎食後3 回に分けて経口投与する。症状により適宜増減する。
必要によって冷水で2 倍程度に希釈して経口投与する。


コメント