Summary
ピタバスタチンを有効成分とする高コレステロール血症治療剤リバロ®の後発医薬品の製造・販売行為がピタバスタチン製剤に関する特許権(特許第5190159号)を侵害するなどと主張して、興和が、東和薬品に対し、損害賠償金等の支払を求めた事件の控訴審。
東和薬品による当該後発医薬品の販売開始(2013年12月)から約9年が経とうとしている。当初の差止請求事件では興和が勝訴しており、その後提起された東和薬品に対する損害賠償請求の総額は約188億円に膨らんでいたが、この損害賠償請求事件において、原審(東京地裁・民事第46部)では東和薬品が逆転勝訴していた。
本控訴審(知財高裁・第2部)も、本件発明は、進歩性欠如が訂正によっても解消されず、無効とされるべきものであるとして、結論において同旨の原判決は相当であり、本件控訴は理由がないからこれを棄却すると判決した(東和薬品の勝訴)。
当初の差止請求事件では興和が勝訴(東和薬品が敗訴)、その後の損害賠償請求事件(本事件)では一転して興和が敗訴(東和薬品が勝訴)となった原因は、侵害論における東和薬品による特許無効の抗弁の内容の違いにあった。
なお、当該控訴審判決は確定し、訴訟は終結した。
1.背景
本件(知財高裁令和4年(ネ)10052)は、ピタバスタチンを有効成分とする高コレステロール血症治療剤リバロ®の後発医薬品の製造・販売行為がピタバスタチン製剤に関する特許権(特許第5190159号に係る請求項6ないし9)を侵害するなどと主張して、興和が、東和薬品に対し、損害賠償金等の支払を求めた事件の控訴審である。
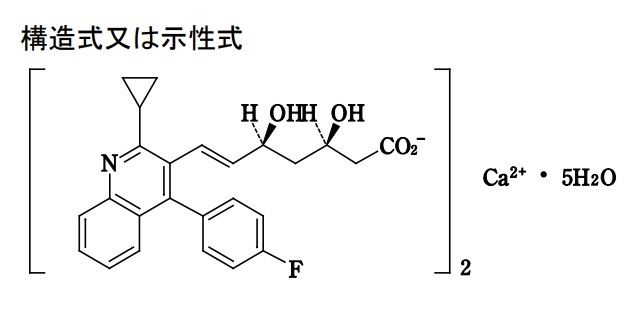 本件発明6及び9は、有効成分であるピタバスタチン又はその塩と、崩壊剤であるカルメロース又はその塩、クロスポビドン並びに結晶セルロースからなる群から選ばれる1種以上を含有する固形薬剤の水分含量を2.9質量%以下とすることにより、HMG-CoA還元酵素阻害活性の低いラクトン体の生成を抑制し、固形製剤中のピタバスタチン又はその塩の安定性を良好にするとともに、崩壊性に優れ、有効成分の放出と薬効発揮を確実にするとの効果を奏するものである。
本件発明6及び9は、有効成分であるピタバスタチン又はその塩と、崩壊剤であるカルメロース又はその塩、クロスポビドン並びに結晶セルロースからなる群から選ばれる1種以上を含有する固形薬剤の水分含量を2.9質量%以下とすることにより、HMG-CoA還元酵素阻害活性の低いラクトン体の生成を抑制し、固形製剤中のピタバスタチン又はその塩の安定性を良好にするとともに、崩壊性に優れ、有効成分の放出と薬効発揮を確実にするとの効果を奏するものである。
なお、東和薬品は、特許庁に対し、本件特許の請求項6ないし9に係る発明について特許無効審判請求をし、興和は、特許庁に対し、請求項6ないし9について訂正請求をした(以下「本件訂正」という。)。
原審・東京地裁(民事第46部)(平成30年(ワ)17586、平成31年(ワ)7191、令和2年(ワ)7989、令和3年(ワ)8097)は、
「本件明細書の記載から、当業者は、本件各発明の固形製剤の水分含量を2.9質量%以下にすれば、結晶セルロースを除いた構成によって、ラクトン体の生成率(40℃75%RH2か月後)が0.23%と0.35%の間のいずれかの値以下に抑制された医薬品を提供することができると認識することはできない。したがって、本件各発明は、サポート要件(特許法36条6項1号)に違反する。・・・本件訂正によって本件各発明のサポート要件違反の無効理由は解消しないというべきである。
以上によれば、本件各発明に係る特許は、特許法36条6項1号に違反し、特許無効審判により無効にされるべきものといえる(同法123条1項4号)から、原告は、同法104条の3第1項により、本件各発明に係る特許権を行使することはできない。」
と判断し、興和の請求を全部棄却したところ、興和は、これを不服として本件各控訴を提起した(なお、興和は、本件特許の請求項7及び8に基づく主張を撤回した。)。
2.裁判所の判断
知財高裁(第2部)は、本件発明6及び9は、進歩性欠如が本件訂正によっても解消されず、無効とされるべきものであるとして、その余の争点について判断するまでもなく、結論において同旨の原判決は相当であり、本件控訴は理由がないからこれを棄却すると判決した。
本件特許の請求項6及び9に係る本件発明及び本件訂正発明と、無効理由(進歩性欠如)において引用発明となった乙12公報(WO2004/071403)に記載された発明(乙12発明)との相違点を以下の表にまとめた。
| 本件発明 | 本件訂正発明 | 乙12発明との相違点 |
|---|---|---|
| 本件発明6 次の成分(A)及び(B): (A)ピタバスタチン又はその塩; (B)カルメロース及びその塩、クロスポビドン並びに結晶セルロース よりなる群から選ばれる1種以上; を含有し、かつ、水分含量が2.9質量%以下である固形製剤。 | 本件訂正発明6 次の成分(A)及び(B): (A)ピタバスタチン又はその塩; (B)カルメロース及びその塩、クロスポビドン並びに結晶セルロース よりなる群から選ばれる1種以上; を含有し、かつ、 (C)水分含量が1.5~2.9質量%である固形製剤であって、かつ、 錠剤であって、気密包装体に収容される固形製剤(但し、固形製剤又は成分(A)の粒子若しくは成分(A)を含む粒子がポリビニルアルコール又はセルロース誘導体をフィルム形成剤として含む材料の層でコーティングされている固形製剤、及び、アルカリ化物質を含まない固形製剤を除く)。 | 本件発明6と乙12発明との相違点 (相違点1) HMG-CoAレダクターゼ阻害剤である化合物について、本件発明6は、「ピタバスタチン又はその塩」であるのに対し、乙12発明は、「アトルバスタチンCa」である点 本件訂正発明6と乙12発明との相違点 相違点1のほか以下の相違点 (相違点2) 本件訂正発明6は、固形製剤がコーティングされていることは特定されておらず、固形製剤又は成分(A)の粒子若しくは成分(A)を含む粒子がポリビニルアルコール又はセルロース誘導体をフィルム形成剤として含む材料の層でコーティングされている固形製剤を除くものであるのに対し、乙12発明は、固形製剤がカルボキシメチルセルロースナトリウム、グリセロール及び水からなる分散物でコーティングされている点 (相違点3) 本件訂正発明6は、アルカリ化物質を含まない固形製剤を除くものであるのに対し、乙12発明は、そのような固形製剤を除くものではない点 |
| 本件発明9 固形製剤が錠剤である、請求項6~8のいずれか1項記載の固形製剤。 | 本件訂正発明9 次の成分(A)及び(B): (A)ピタバスタチン又はその塩; (B)クロスポビドン; を含有し、 (C)カルメロース及びその塩並びに結晶セルロースをいずれも含有せず、かつ、水分含量が1.5~2.9質量%である固形製剤であって、かつ、錠剤であって、気密包装体に収容される固形製剤(但し、固形製剤又は成分(A)の粒子若しくは成分(A)を含む粒子がポリビニルアルコール又はセルロース誘導体をフィルム形成剤として含む材料の層でコーティングされている固形製剤を除く)。 | 本件発明9と乙12発明との相違点 (相違点1) 同上 本件訂正発明9と乙12発明との相違点 相違点1ないし3のほか以下の相違点 (相違点4) 本件訂正発明9は、「クロスポビドンを含有し、カルメロース及びその塩並びに結晶セルロースをいずれも含有」しないのに対し、乙12発明は、「Prosolv SMCC90」及び「架橋カルボキシメチルセルロース」を含有する点 |
(1)本件発明6の相違点1に係る構成の容易想到性と効果について
裁判所は、
「・・・HMG-CoAレダクターゼ阻害剤である化合物に関し、乙12発明の「アトルバスタチンCa」に代えて、薬効もラクトン体の生成及び抑制の機序も同じである「ピタバスタチン又はその塩」とすることは、本件出願日当時の当業者が適宜なし得たことであると認めるのが相当である。」
と判断した。
また、本件発明6の効果について、裁判所は、
「・・・本件発明6は、HMG-CoA還元酵素阻害活性の低いラクトン体の生成を抑制するとともに、崩壊性に優れるとの効果を奏するものである。この点に関し、乙12公報(実施例8)にも、水分含量を抑えた錠剤において本件相関関係が認められる旨の記載があるところ、本件明細書の記載(試験例1及び2)は、水分含量を2.9重量%以下とすることによって初めて本件相関関係が認められることを示すものではない。
また、本件発明6の「カルメロース及びその塩、クロスポビドン並びに結晶セルロースよりなる群から選ばれる1種以上」とは、崩壊剤(本件崩壊剤)として用いられるものを指すところ・・・、本件崩壊剤を混合して得られた本件混合物又は本件混合物に係る固形製剤若しくは医薬品である本件混合物等(本件発明6)が崩壊性に優れることは、自明のことである。
そうすると、本件発明6の上記各効果は、本件出願日当時の当業者が乙12発明から予測し得た範囲内のものにすぎないというべきであり、これが格別顕著なものであるということはできない。」
と判断した。
(2)本件訂正発明6の相違点2及び相違点3に係る構成の容易想到性と効果について
ア 相違点2
裁判所は、
「乙12発明における「コーティング」は、酸化や環境湿度等に敏感なスタチン類(HMG-CoAレダクターゼ阻害剤)を保護し、これを安定化するために塗布される材料の層であるところ、従来から、固形医薬品の安定性を高める目的で保護コーティングが施され、その材料として様々なもの(ポリビニルアルコール又はセルロース誘導体ではないアミノアルキルメタアクリレートコポリマーEを含む。)が開発されていることが周知であり、特に、HMG-CoA還元酵素阻害剤のコーティング材料として、カルメロース及びその塩、クロスポビドン等の崩壊剤と共に、アミノアルキルメタアクリレートコポリマーEを用い得ることが知られていたものと認めることができる。
そうすると、乙12発明の「コーティング」の材料として、「カルボキシメチルセルロースナトリウム、グリセロール及び水からなる分散物」に代え、アミノアルキルメタアクリレートコポリマーE等の「ポリビニルアルコール又はセルロース誘導体」を含まない周知のものを採用することは、乙12公報に接した本件出願日当時の当業者において適宜なし得たことであると認めるのが相当である。」
と判断した。
イ 相違点3
裁判所は、乙12発明において「アルカリ化物質」を含む固形製剤とすることも、本件出願日当時の当業者が容易になし得たことであると認めるのが相当であると判断した。
ウ 効果について
裁判所は、
「本件訂正発明6は、本件発明6が奏する効果に加え、固形製剤が気密保存可能な包装体によって包装されることにより包装体の内部に水分が浸入することが妨げられるため、長期間にわたって包装体の内部の固形製剤の水分含量が安定的に保たれ、もって、固形製剤中におけるピタバスタチン又はその塩に由来するラクトン体の生成が長期間にわたって抑制され、また、水分含量が1.5質量%以上の場合、5-ケト体の生成も抑制され、固形製剤中のピタバスタチンの安定性を特に良好にするという効果を奏するものと認められる。」
とした上で、固形製剤を気密包装体に収容することによる効果及び5-ケト体の生成を抑制するとの効果についても、本件出願日当時の当業者が知られていた技術的事項に基づいて予測することのできる範囲内のものであって、これが格別顕著なものであるということはできないと判断した。
(3)本件訂正発明9の相違点4に係る構成の容易想到性と効果について
裁判所は、
「乙12発明につき、崩壊剤として「クロスポビドン」を含有し、「カルメロース若しくはその塩又は結晶セルロース」を含有しないとすることは、本件出願日当時の当業者が容易に想到し得たものであると認めるのが相当である。なお、乙12公報には、フィラー及びバインダーとして、「結晶セルロース(MCC)」等を例示する各記載(前記3(1)ク)があるが、これらの記載も、乙12公報に記載された医薬剤形がカルメロース若しくはその塩又は結晶セルロースを含有することを要件とする旨を開示するものではない。
・・・本件訂正発明9が本件訂正発明6と異なる効果を奏する旨の主張はないところ、前記・・・のとおり、本件訂正発明6の効果は、本件出願日当時の当業者が予測することのできる範囲内のものであって、これが格別顕著なものであるということはできないから、本件訂正発明9の効果も、本件出願日当時の当業者が予測することのできる範囲内のものであって、これが格別顕著なものであるということはできない。」
と判断した。
3.コメント
原審・東京地裁では、サポート要件違反で本件特許は無効とされるべきであり、本件各発明に係る特許権を行使することはできないとして興和の請求を棄却したが、控訴審である知財高裁は、進歩性欠如を理由として本件特許は無効とされるべき、さらに本件訂正によってもそれは解消されないとして、その余の争点について判断するまでもなく、結論において同旨の原判決は相当であり、本件控訴は理由がないからこれを棄却すると判決した。
当初、東和薬品による後発医薬品の製造販売行為に対する特許権侵害に基づく差止請求事件では、興和が勝訴(東和薬品が敗訴)していた。その後、同特許権侵害に基づく損害賠償請求を定期で繰り返すなど、一方的な勢いを見せていた興和だったが、この損害賠償請求事件(本事件)では、一転、原審に続いて控訴審でも興和が敗訴(東和薬品が勝訴)となった。
この逆転の決め手は何だったのだろうか。この点に興味がある。
以下に、その点に焦点を当てて経緯を振り返った。
興和と東和薬品との間のピタバスタチン特許権侵害紛争は2013年の東和薬品による後発医薬品(先発品は興和のリバロ®)の販売開始に遡る。
- 2013年12月、東和薬品は、『ピタバスタチン Ca・OD錠 4mg「トーワ」』の販売を開始した。
- 興和は、2015年10月30日付にて東和薬品に対し、本件特許(第5190159号)に係る特許権の侵害を理由として『ピタバスタチン Ca・OD錠 4mg「トーワ」』の製造販売の差し止めを求める訴訟を東京地裁に提起し、東京地裁(民事第29部)は興和の請求を全面的に認める判決を下した(2017.09.29 「興和 v. 東和薬品」 東京地裁平成27年(ワ)30872)。この事件で、東和薬品は、先使用の抗弁及び特許無効の抗弁(興和自身が特許権者である特許第4981194号公報(乙7公報)による進歩性欠如)を主張している。しかし、進歩性については、乙7公報のピタバスタチン固形製剤の水分含量を「1.5~2.9質量%」の数値範囲内とすることが容易であったとは認めることは困難と判断された。また、東和薬品は、特許無効の抗弁において、サポート要件違反の主張をしていない。
- その後、東和薬品による知財高裁(第4部)への控訴も棄却され(2018.04.04 「東和薬品 v. 興和」 知財高裁平成29年(ネ)10090)、さらに東和薬品による最高裁への上告受理申立は不受理(2019年2月14日)となり、製造販売の差し止め判決は確定した。
- 2018年6月1日、興和は、上記の差止請求訴訟における知財高裁での勝訴判決を受けて、東和薬品による後発医薬品の販売行為(2013年12月13日から2016年3月31日まで)が興和の製剤特許の侵害にあたると主張して、東和薬品に対して損害賠償請求訴訟を東京地裁に提起した(請求金額は約38億円)。その後、2019年3月22日には、2016年4月から1年間の販売分(請求金額は約45億円)、2020年3月25日には、2017年4月から1年間の販売分(請求金額は約48億円)、2021年3月30日には、2018年4月から1年間の販売分(請求金額は約56億円)に対する損害賠償請求訴訟を毎年追加的に東京地裁に提起した。興和から東和薬品への損害賠償請求額は総額で約188億円まで膨らんだ(2021.04.06記事: 東和薬品のピタバスタチンOD錠 興和が製剤特許侵害で、さらに追加の損害賠償請求)。
- 一方、東和薬品は、上記の差止請求事件における知財高裁での敗訴判決を受けて、2018年7月19日、本件特許に対する無効審判を特許庁に請求した(無効2018-800092)。同年11月22日、この審判手続きにおいて、東和薬品から乙12公報(WO2004/071403)(審判事件弁駁書1・甲第12号証)等が提出された。ここで潮目が変わる。東和薬品は、この無効審判請求事件及び損害賠償請求事件からは製薬業界・技術に詳しいと思われる弁護士や弁理士をそれら事件の代理人として採用している。個人的にはこの点がその後の形勢逆転の大きな要因になったと見ている。
- 2020年9月18日、同公報に基づき本件発明1及び2の特許は無効であるとの審決を勝ち取り、その後当該審決は確定した。
- その後、2020年12月17日、本件特許の残る請求項について、東和薬品は、無効審判を特許庁に請求し(無効2020-800121)、その審決の予告(2022年6月17日)において、特許庁は、乙12公報に基づく進歩性欠如及びサポート要件違反等の理由により対象となる請求項に係る特許は無効であるとの判断を示したところである。
- ここで、また前述の損害賠償請求訴訟に戻る。2022年3月24日、東京地裁(民事第46部)が、本件特許はサポート要件違反により無効とされるべきものであるとして、興和の請求を棄却する判決を言い渡し、東和薬品の勝訴となった(2022年3月24日の東和薬品のプレスリリース(ピタバスタチン Ca・OD 錠「トーワ」の損害賠償請求訴訟における勝訴判決のお知らせ)(平成30年(ワ)17586、平成31年(ワ)7191、令和2年(ワ)7989、令和3年(ワ)8097)。
- 2022年4月6日、興和は、これを不服として、知財高裁に控訴した(興和 高コレステロール血症治療剤リバロ®の後発医薬品を製造販売した東和薬品に対する損害賠償請求訴訟で特許無効により敗訴、知財高裁に控訴へ)。
- 2022年9月21日、控訴審(知財高裁第2部)においても、本件特許が無効(進歩性欠如による)とされるべきものとの判断に基づき興和の請求を棄却した一審判決を支持する内容で、再び東和薬品が勝訴判決を受けた(興和 高コレステロール血症治療剤リバロ®の後発医薬品を製造販売した東和薬品に対する損害賠償請求訴訟 知財高裁も特許無効と判断し東和薬品の勝訴判決)。
以上のとおり、当初差止請求事件では興和が勝訴(東和薬品が敗訴)、その後の損害賠償請求事件(本事件)では一転して興和が敗訴(東和薬品が勝訴)となった原因は、侵害論における東和薬品による特許無効の抗弁の内容の違いにあったといえるが、それを導き出せたのは、東和薬品の代理人として新たに委任された弁護士・弁理士の力量によるものであったのではないだろうか、と想像する。
なお、上告期限である10月5日までに興和が上告及び上告受理申立てを行わなかったため、東和薬品の勝訴判決が確定し、訴訟は終結した。
- 2022.10.06 東和薬品 press release: 当社に対する訴訟の終結に関するお知らせ



コメント
無効2018-800092で、なぜ興和は審決取消訴訟を提起していないのでしょうか。
コメントありがとうございます。
差止請求が認められたのは請求項2に基づく侵害でしたので、裁判所の判断を仰いで早期決着を望むなら、ご指摘のとおり審決取消訴訟を提起して争いつづけても良かったとも思います。
しかし、興和が審決取消訴訟を提起しなかったのは、全ての請求項が無効にされたわけではないからかもしれません。例えば請求項6とかはもともと同審判では無効請求されておらず、その請求項が残っていれば同様に侵害判断を得られる(かもしれない)から(2018年6月1日に提起した損賠賠償請求では請求項6ないし9で勝負してきていますし)、敢えて請求項1及び2に拘らなかったのかもしれませんね(いざとなったら残った請求項の訂正の機会もあるわけですし)。
むしろ、東和薬品がなぜ早期にしかも最初の無効審判で請求項6等も含めて無効請求していなかったのかが不思議に思います。
東和が請求項6等について無効審判請求をしなかったのは、侵害訴訟で興和が侵害を主張していなかったからだと推測しますが、差止請求が認められた請求項を興和があっさり諦めてしまったところにちょっと違和感を感じました。審決取消訴訟を提起しながらも、請求項6で損害賠償請求もできたように思えますし・・・
ご指摘のとおり違和感ありますね・・・元をたどると興和が請求項6等でも全力で差止請求しなかったことも違和感が。権利行使の小出し作戦なのでしょうか。意図的なのだと思いますが、その時点から何か複雑というか非効率な訴訟の応酬に感じられてきました。ご指摘ありがとうございます。