レボフロキサシン(クラビット)の特許権存続期間延長登録に無効判決: 知財高裁平成20年(行ケ)10486
【背景】
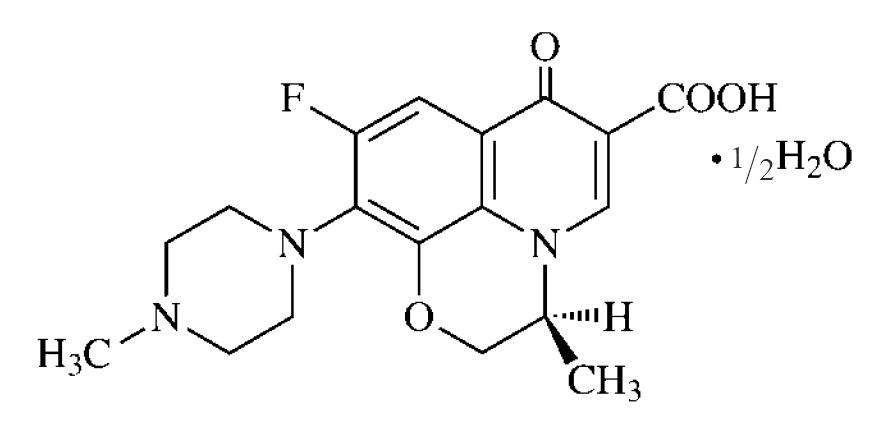 第一製薬はクラビット(Cravit)(有効成分はレボフロキサシン(levofloxacin))の〈適応菌種〉レジオネラ属の効能追加承認に基づいて特許権(1659502)の存続期間延長登録(延長登録出願番号: 2006-700042; 延長された期間: 4年11月7日)をした。しかし、後発品メーカー13社が起した延長登録無効審判によって、2年6月5日(本件国内臨床試験開始日から本件承認了知日の前日までの期間)を超える期間の延長登録を無効とする審決(無効2007-800168)が下されたため、第一三共は審決取消訴訟を提起した。
第一製薬はクラビット(Cravit)(有効成分はレボフロキサシン(levofloxacin))の〈適応菌種〉レジオネラ属の効能追加承認に基づいて特許権(1659502)の存続期間延長登録(延長登録出願番号: 2006-700042; 延長された期間: 4年11月7日)をした。しかし、後発品メーカー13社が起した延長登録無効審判によって、2年6月5日(本件国内臨床試験開始日から本件承認了知日の前日までの期間)を超える期間の延長登録を無効とする審決(無効2007-800168)が下されたため、第一三共は審決取消訴訟を提起した。
過去記事参照:
【要旨】
2. 取消事由2(本件米国臨床試験の実施期間を延長期間に算入しなかった誤り)について
特許発明の存続期間の延長登録制度の趣旨について、裁判所は、下記のように言及した。
「特許法は,特許権者が,許可を得ようとしなかった期間も含めて,特許発明を実施することができなかったすべての期間(ただし,5年の限度以内である。)について,存続期間延長の算定の基礎とするのではなく,特許発明を実施する意思及び能力があってもなお,特許発明を実施することができなかった期間,すなわち,当該「政令で定める処分」を受けるために必要であった期間に限って,存続期間延長の対象としている。」
そして、本件の「特許発明の実施をすることができない期間」該当性に関して、裁判所は、
「①米国の効能追加承認においては米国初回臨床試験の10症例の成績のみでレジオネラ肺炎に対する効能・効果の追加承認がされており,本件米国臨床試験は必要とされなかったのであるから,その後に申請される日本での同様のレジオネラ肺炎に対する効能・効果の追加承認においても,米国初回臨床試験のデータのみがあれば足り,本件米国臨床試験は必ずしも必要とはされなかったであろうと合理的に推認することができ,
②本剤と同じフルオロキノロン系薬の1つであるメシル酸パズフロキサシンのレジオネラ肺炎に対する効能・効果の追加に関する上記審査において,本件承認申請と極めて類似した状況の下で効能追加の承認がされたことからすると,メシル酸パズフロキサシンの6症例を上回る10症例に係る臨床試験データを有する米国初回臨床試験があれば,本件米国臨床試験データがなくとも,日本での本剤の効能追加の承認がされたであろうと合理的に推認することができる。」
と判断した。
原告は、
「メシル酸パズフロキサシン(甲10)は,経口剤よりも即効性の高いレジオネラ肺炎に対する国内唯一の注射剤であって,致命的な疾患であるレジオネラ肺炎について医療上の緊急性から極めて例外的に承認されたにすぎず,既にレジオネラ肺炎に対する効能が承認済みの他の経口抗菌剤が存在する状況の下では,経口剤である本剤の承認申請については,メシル酸パズフロキサシンと同様の審査がされて承認されたであろうとはいえない」
と主張した。
しかし裁判所は、
「致命的な疾患であるレジオネラ肺炎を適応とする点では本剤もメシル酸パズフロキサシンも同じであるから,原告の上記主張は前記の合理的推認を覆すに足りない。」
と判断した。
3. 取消事由3(日本の承認に向けた活動再開日から本件国内臨床薬理試験開始日までの期間を延長期間に算入しなかった誤り)について
裁判所は、
「前記2で説示したとおり,本件米国臨床試験に係る期間は,特許法67条2項にいう「政令で定めるものを受けることが必要であるために,その特許発明の実施をすることができない期間」には当たらないから,同期間に該当することを前提として,本件米国臨床試験を一時中断した後に再開した日を,同期間の再開日に該当するものということはできない。」
と判断した。
原告は、
「実際の治験計画届の提出前には,医薬当局と新たな臨床試験が必要かどうか,どのような枠組みで承認申請をするかなどの協議をしたり,臨床試験を実施してくれる医師を探して依頼したりする作業期間が必要であり,これらの準備作業をした平成14年12月19日以降の期間は,実質的にみても,「政令に定めるものを受けることが必要であるため,その特許発明の実施をすることができない期間」の起算日(承認を受けるのに必要な試験を開始した日)に該当するというべきである」
と主張した。
しかし、裁判所は、
「準備がいつどのように開始され,継続されるのかは第三者にとって必ずしも明確ではない。したがって,仮に,不明確な準備作業の開始日をもって「承認を受けるのに必要な試験を開始した日」(最高裁判所平成10年(行ヒ)第43号平成11年10月22日第二小法廷判決参照)に該当するとするならば,延長登録期間の客観的な確定を困難にさせ,予見可能性を担保することができなくなる。したがって,臨床試験を実施することが治験計画届や治験を実施する医療機関との契約書等により客観的に明確になった日をもって,「承認を受けるのに必要な試験を開始した日」であるとして,「政令に定めるものを受けることが必要であるため,その特許発明の実施をすることができない期間」の進行が開始するものとするのが相当である。
これを本件についてみると,本件国内臨床薬理試験の治験届が提出された日である平成15年8月29日をもって,「承認を受けるのに必要な試験を開始した日」に当たるものと認めるのが相当であり,本件において,この認定を左右するに足りる証拠はない。したがって,これと結論を同じくする審決の判断は正当であり,この点に係る原告の上記主張は理由がない。」
と判断した。
請求棄却。
【コメント】
本判決が意味するところは、「特許発明の実施をすることができない期間」に該当するというためには、海外臨床試験・国内臨床試験のいずれを問わず、承認を受けることが必要なために費やされた期間だったことを合理的に説明できなければならないこと、及び、その期間の開始日(及び終了日)を客観的に示すことができなければならない、ということだろう。
ところで、第一三共は本件特許権存続期間延長登録に基づいて侵害訴訟を提起している。
- 2009.04.09 「Daiichi Sankyo Files Patent Infringement Actions against 11 Generics Companies for CRAVIT® TABLETS and FINE GRANULES」
- 2009.03.23 「Daiichi Sankyo Files Patent Infringement Actions against 13 Generics Companies for CRAVIT® TABLTETS and FINE GRANULES」
その他の関連記事:
- 2009.04.22 第一三共 新用法・用量クラビット製剤承認
- Levofloxacin – Thirteen generic companies file request for invalidation of Daiichi’s patent term extension.
- 沢井製薬プレスリリース: 2009.10.28 レボフロキサシン審決取消訴訟の勝訴に関するお知らせ
- 大洋薬品プレスリリース: 2009.10.28 レボフロキサシン特許延長にかかる訴訟で判決言渡


コメント