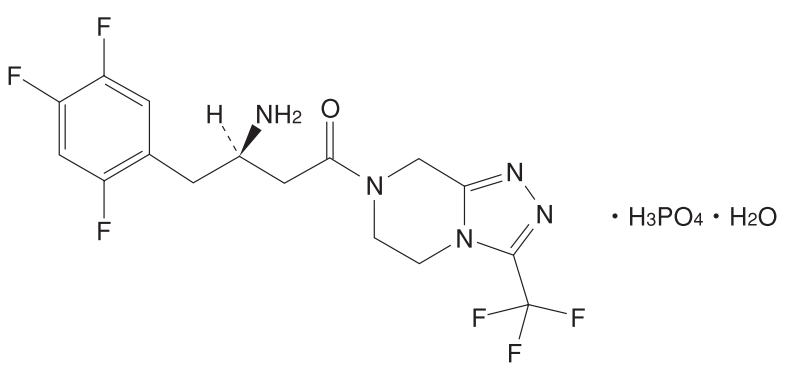
 ジャヌビア®錠100mg/50mg/25mg/12.5mg(一般名:シタグリプチンリン酸塩水和物, Sitagliptin Phosphate Hydrate)の後発医薬品であるメディサ新薬株式会社(サワイグループホールディングス株式会社の子会社、以下「メディサ新薬」)のシタグリプチン錠100mg/50mg/25mg/12.5mg「サワイ」(以下「シタグリプチン製剤」)が2023年8月15日に製造販売承認されていましたが、2023年10月26日のMSD株式会社のプレスリリースによると、メディサ新薬によるシタグリプチン製剤の製造販売行為は、特許第3762407号に係る特許権を侵害するものであるとして、Merck Sharp & Dohme LLCが、2023年10月6日、沢井製薬株式会社とメディサ新薬に対し、特許権侵害訴訟および仮処分申請を東京地方裁判所に提起したとのことです。
ジャヌビア®錠100mg/50mg/25mg/12.5mg(一般名:シタグリプチンリン酸塩水和物, Sitagliptin Phosphate Hydrate)の後発医薬品であるメディサ新薬株式会社(サワイグループホールディングス株式会社の子会社、以下「メディサ新薬」)のシタグリプチン錠100mg/50mg/25mg/12.5mg「サワイ」(以下「シタグリプチン製剤」)が2023年8月15日に製造販売承認されていましたが、2023年10月26日のMSD株式会社のプレスリリースによると、メディサ新薬によるシタグリプチン製剤の製造販売行為は、特許第3762407号に係る特許権を侵害するものであるとして、Merck Sharp & Dohme LLCが、2023年10月6日、沢井製薬株式会社とメディサ新薬に対し、特許権侵害訴訟および仮処分申請を東京地方裁判所に提起したとのことです。
また、日本でシタグリプチンの後発医薬品の承認を取得(もしくは申請)したと報道されている後発医薬品企業とMSD株式会社の間にライセンス契約や許諾は存在していないとのことです。
参照:
- 2023.10.26 MSD株式会社 press release: シタグリプチンの知的財産権保護に関する訴状と仮処分申請を提出
シタグリプチンの物質特許第3762407号(20年の満了日: 2022年7月5日)は、ジャヌビア®錠について延長された存続期間が2025年2月21日~2026年3月30日(効能・効果による)まで存続しています。
「医療用後発医薬品の薬事法上の承認審査及び薬価収載に係る医薬品特許の取扱いについて(各都道府県衛生主管部(局)長あて厚生労働省医政局経済課長・厚生労働省医薬食品局審査管理課長通知)(平成21年6月5日付け医政経発第0605001号/薬食審査発第0605014号)」及び「承認審査に係る医薬品特許情報の取扱いについて(平成6年10月4日付け薬審第762号審査課長通知)」において、後発医薬品の薬事法(現・薬機法)上の承認審査にあたっては、
- 先発医薬品の有効成分に特許が存在する場合には後発医薬品を承認しないこと
- 先発医薬品の特許が存在する効能・効果、用法・用量(効能・効果等)については承認しない方針であること
- 特許の存否は承認予定日で判断するものであること
を従前より定めており、この厚生労働省からの通知(以下、「二課長通知」という。)に従えば、今回のメディサ新薬によるシタグリプチン製剤の製造販売承認は、前記延長された特許権の存在により本来承認されないはずです。
しかし、先発医薬品であるジャヌビアⓇ錠の有効成分は「シタグリプチンリン酸塩水和物」として錠剤に含有されているのに対し、メディサ新薬のシタグリプチン製剤の有効成分は「シタグリプチンリン酸塩(無水物)」であるという違いがあります。
ジャヌビアⓇ錠の物質特許に係る特許権はその存続期間が延長されたため現在も存続していますが、もしかすると、厚生労働省は、有効成分が「シタグリプチンリン酸塩水和物」として含有されている先発医薬品ジャヌビアⓇ錠について延長された特許権の効力が、有効成分が「シタグリプチンリン酸塩(無水物)」として含有されている後発医薬品に及ぶのかどうか判断できず、二課長通知の運用(パテントリンケージ)を機能させることをあきらめて当事者間での特許紛争に委ねたのではないかと推測されます。
なお、承認申請の審査上、水和物/無水物の違いがあっても、それは同じ有効成分として取り扱われることが規定されており(平成23年6月16日付け薬食審査発0616第1号 厚生労働省医薬食品局審査管理課長通知「異なる結晶形等を有する医療用医薬品の取扱いについて」)、これを踏まえれば、ジャヌビアⓇ錠とメディサ新薬のシタグリプチン製剤との間に水和物/無水物の違いがあろうとも、厚生労働省は同じ有効成分として取り扱っているはずであり、その一方で、厚生労働省が二課長通知の運用(パテントリンケージ)を機能させなかったことには大きな違和感があるように思われます。このような運用事例は、沢井製薬株式会社のダサチニブ錠の効能追加承認でも見られています(2023.10.17記事: ブリストル・マイヤーズ スクイブが沢井製薬ダサチニブ錠の効能追加販売に対し特許権侵害の差止仮処分命令申立て)。
厚生労働省の今回の二課長通知の運用(パテントリンケージ)は、当事者間の紛争に収まらず、業界全体において大きな議論を生むかもしれません。

この訴訟は、よくある後発品を巡る特許侵害訴訟と思っていたら大間違い。これはTPP11で義務化されている日本のパテントリンケージ運用のあり方と延長された特許権の効力という、製薬企業にとって超重要な制度の二大問題が同時に試されている案件ですよ!
参照:
- 日本のパテントリンケージの現状の課題とその解決に向けた提案
- 【アンケート】パテントリンケージとして運用されている二課長通知の問題点は何だと思いますか?
- ジェネリック医薬品と特許(gemedicines): シタグリプチン(投稿日: 2023年9月16日、URL: https://gemedicines.blogspot.com/2023/09/blog-post.html)
- 2023.10.17記事: ブリストル・マイヤーズ スクイブが沢井製薬ダサチニブ錠の効能追加販売に対し特許権侵害の差止仮処分命令申立て
- 2021.03.02記事: 武田と帝人ファーマ、糖尿病薬4剤の販売移管・資産譲渡契約を締結・・・特許独占期間と他社DPP4阻害薬ジェネリック参入時期のインパクト

コメント
2023年12月7日、厚労省は後発医薬品などの薬価基準追補収載を官報告示。ジャヌビア®にとっての初の後発医薬品となる8月に承認された『シタグリプチン錠100mg/50mg/25mg/12.5mg「サワイ」』は、官報にその記載はなく、収載は見送られました。
https://kanpou.npb.go.jp/20231207/20231207g00256/20231207g002560004f.html
2025年2月17日、厚労省は、第一三共エスファによる『シタグリプチン錠100mg/50mg/25mg/12.5mg「DSEP」』(ジャヌビア®錠の後発医薬品)を承認した。オーソライズドジェネリックかもしれない?