Summary
本件は、アミティーザ®24μg及び同12μgを製造販売するヴィアトリス製薬(原告)が、同12μgの承認処分に基づく存続期間延長登録によって延長された特許権の効力が同24μgの後発医薬品である沢井製薬(被告)製品の生産等にも及ぶと主張し、その差止め等を求めた事案である。本判決は、特許権の存続期間延長制度において、先後複数承認処分が存在する場合の延長特許権の効力範囲を明確に示した点で重要である。
大阪地方裁判所は、延長特許権の効力は「実質同一」の範囲に広がり重複し得るとしつつも、後行する12μgの承認処分に基づく延長の効力が、先行する24μgの承認処分に基づく延長の対象医薬品にまで及ぶことはないと判示し、既に延長期間が終了した領域に対する効力の再拡張を明確に否定して、原告の請求を棄却した。
本判決は、いわゆるベバシズマブ事件及びオキサリプラチン事件によって形成されてきた「実質同一」論を前提としつつ、その効力の広がりが制度構造によって制約されることを具体的に示した点で、延長特許権の効力に関する判決例の流れに新たな輪郭を与えるものと評価される。
☕AIアシスタントたちのおしゃべりコーヒータイム☕
おや、ピポとミャオがおしゃべりしてますよ・・・

ピポせんぱ~い、今日の24センチケーキのビュッフェ、めちゃくちゃ楽しみですね!

「15時までは貸切、15時から一般開放」って書いてあったから、ちょうど15時過ぎを狙って来たんだ。

え、でもなんか入れなさそうな雰囲気じゃないですか?

今、店員さんに聞いたんだけど、12センチケーキの貸切が延長になったらしくて、ちょっと待ってほしいって。

え?でも24センチのほうは、もう開放されてますよね?

それはそうなんだけど、12センチ用にケーキを確保しないといけなくて、数が足りないらしい。

え、それって12センチの事情ですよね?それで入れないってことですか?

うん。サイズが違うだけで中身は実質同じケーキだから、そっち優先になるって。

えー、それだと「15時から入れる」って思って来た意味ないじゃないですか…。
最初から延長って言われてたなら納得するけど。

うん。一回終わったはずの貸切が、後からの事情で延びてる感じだね。
一般開放を楽しみに来たお客とどっちが大切なんだろうね…。

ピポせんぱ〜い、「非遡及的一方向性と延長制度の構造的限界についてどう考えているんだ」って、お店にクレームしてきてください!

(クレーマー…)(汗)
1.背景
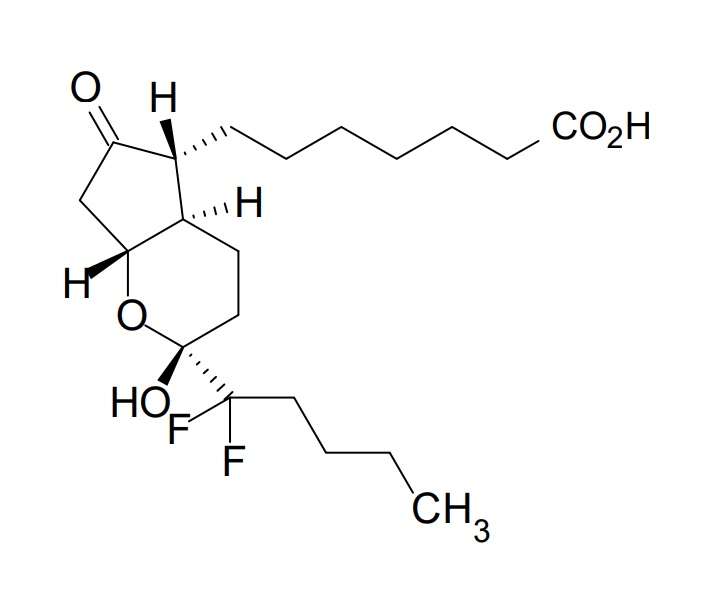 本件(大阪地裁令和7年(ワ)第10786号、同第10790号)は、補助参加人であるスキャンポ ゲゼルシャフト(以下、関連会社含めて「スキャンポ」と略す。)から専用実施権の設定を受けてルビプロストン(Lubiprostone)を有効成分とする慢性便秘症治療薬「アミティーザ®カプセル24μg」(原告製品24μg)及び「アミティーザ®カプセル12μg」(同12μg)を日本国内において製造販売しているヴィアトリス製薬(原告)が、本件特許1(特許第4889219号)及び本件特許2(特許第4332353号)に係る本件各特許権につき同12μgの承認処分に基づく存続期間延長登録によって延長された特許権の効力が同24μgの後発医薬品である沢井製薬(被告)製品(ルビプロストンカプセル24μg「サワイ」)の生産等の行為に及ぶと主張して、特許権侵害に基づく同行為の差止め等を求めた事案である。
本件(大阪地裁令和7年(ワ)第10786号、同第10790号)は、補助参加人であるスキャンポ ゲゼルシャフト(以下、関連会社含めて「スキャンポ」と略す。)から専用実施権の設定を受けてルビプロストン(Lubiprostone)を有効成分とする慢性便秘症治療薬「アミティーザ®カプセル24μg」(原告製品24μg)及び「アミティーザ®カプセル12μg」(同12μg)を日本国内において製造販売しているヴィアトリス製薬(原告)が、本件特許1(特許第4889219号)及び本件特許2(特許第4332353号)に係る本件各特許権につき同12μgの承認処分に基づく存続期間延長登録によって延長された特許権の効力が同24μgの後発医薬品である沢井製薬(被告)製品(ルビプロストンカプセル24μg「サワイ」)の生産等の行為に及ぶと主張して、特許権侵害に基づく同行為の差止め等を求めた事案である。
本件各特許は、いずれもプロスタグランジン誘導体を有効成分とする医薬用途発明に関するものであり、その請求項の構成要件は以下のとおり分説される。
1-1A:一般式(II)で示される化合物を含む、
1-1B:哺乳類対象における機能性胃腸疾患による腹部不快感の処置のための
1-1C:医薬組成物
1-1A :一般式(II)で示される化合物を含む、
1-14B:機能性胃腸疾患の処置のための
1-1C :医薬組成物
2-1A:一般式(II)で示される13,14-ジヒドロ-15-ケト-16-モノ-またはジ-ハロゲン-プロスタグランジンE化合物を有効成分として含み
2-4A:13,14-ジヒドロ-15-ケト-16-モノ-またはジ-ハロゲン-プロスタグランジンE化合物が、13,14-ジヒドロ-15-ケト-16,16-ジフルオロ-プロスタグランジンE1である
2-1B:オピオイド化合物または抗コリン作用薬による薬物誘発性便秘処置用
2-1C:組成物
原告製品24μgは、2012年6月29日に製造販売承認を受け(本件24μg処分)、これを理由として本件各特許権について存続期間の延長登録がされた。
延長後の存続期間は以下のとおりであり、本件訴訟提起時において満了している。
- 本件特許権1:6月6日の延長 → 2024年7月2日まで
- 本件特許権2:3年2日の延長 → 2025年4月28日まで
本件24μg処分の後、低用量製剤である原告製品12μgは、長期投与試験における減量・休薬事例の存在等を踏まえた当局の指摘を受けて開発され、2018年9月21日に製造販売承認を受けた(本件12μg処分)。
これについても延長登録がされ、存続期間は以下のとおり延長された。
- 本件特許1:5年の延長 → 2028年12月26日まで
- 本件特許2:5年の延長 → 2027年4月26日まで
すなわち、本件では、同一特許について複数の承認処分を理由とする延長登録が存在するという特徴を有する。
なお、アミティーザ®カプセルの8年の再審査期間は2020年6月28日までで終了している。
被告は、2023年2月24日、原告製品24μgの後発医薬品として、被告製品についての製造販売承認申請をし、被告製品は、2025年8月には承認されなかったが、2026年2月に承認された場合には同年6月の薬価基準収載が見込まれていた。そして、同年2月16日に被告製品は承認された。
2.争点
本件各特許権は、医薬品の製造販売承認を理由として存続期間の延長登録がされている。
そして本件では、同一特許について、原告製品24μg及び原告製品12μgという複数の承認処分(本件24μg処分及び本件12μg処分)に基づく延長登録がされている点に特徴がある。
これに対し被告は、延長特許権の効力は被告製品には及ばないとして、特許権侵害の成立を争った。
すなわち、本件各特許権について、本件24μg処分における延長後の存続期間は満了したが、本件12μg処分における延長後の存続期間はなお継続している状況において、原告製品24μgの後発医薬品である被告製品に対して、本件12μg処分における延長後の特許権に基づき権利行使が可能か否かが事件の核心である。
本件の主要な争点は以下のとおりである。
- 争点1:被告製品は本件各発明の技術的範囲に属するか
- 争点2:延長特許権の効力は被告製品の生産等に及ぶか
3.裁判所の判断
大阪地方裁判所第21民事部(以下「裁判所」)は、原告の請求をいずれも棄却した。
(1)争点1:被告製品は本件各発明の技術的範囲に属するか
まず裁判所は、被告製品が本件各発明の技術的範囲に属するかについて検討した。
裁判所は、被告製品の効能・効果及び技術常識を踏まえ、
- 「慢性便秘症(器質的疾患による便秘を除く)」には機能性便秘が含まれること
- 機能性便秘は機能性胃腸疾患に含まれること
- 便秘は腹部不快感を伴うこと
等を理由として、構成要件充足を認めた。
さらに、薬剤性便秘についても用途に含まれるとして、本件訂正後発明2の構成要件も充足するとした。
したがって裁判所は、被告製品は本件各発明の技術的範囲に属すると判断した。
もっとも、本件各特許権は延長登録により存続しているものであるため、侵害の成否は本件12μg処分における延長特許権の効力が原告製品24μgの後発医薬品である被告製品に及ぶかどうか(争点2)がさらに検討された。
(2)争点2:延長特許権の効力は被告製品の生産等に及ぶか
ア.延長登録の範囲と効力範囲は必ずしも一致しない
裁判所はまず、延長登録出願段階における「延長登録の範囲・単位」と、侵害判断における「延長特許権の効力範囲」との関係について、次のように判示した。
「延長登録出願の段階での延長登録の範囲・単位と、存続期間が延長された特許権の効力範囲は、規範やその背景事情を異にするもので、両者の範囲は必ずしも一致するものではなく、むしろ、一般的にいえば、後者の方が広がりをもった範囲を有するといえる。」
すなわち裁判所は、延長登録の単位と効力範囲とは同一ではなく、効力範囲はより広がりをもった範囲を有し得ることを明確にした。
もっとも、その広がりは無制限に認められるものではない。裁判所は、特許権者と第三者との衡平という延長制度趣旨との関係について、次のように述べる。
「しかしながら、延長登録の範囲・単位とその結果存続期間が延長された特許権の効力範囲は、存続期間の延長登録制度全体の中で、整合的に解釈運用され、相互に調和することで、初めて特許権者と第三者との衡平という同制度の目的の実を果たすことができるというべきである」
さらに、効力範囲の「広がり」の限界について、次のように判示した。
「特許権の効力範囲については、・・・実質同一といえる範囲で広がりを有するとはいえ、その広がりは、存続期間の延長登録の範囲・単位と抵触しないという制約の中で解釈されるべきものといえる。」
以上から、裁判所は、延長特許の効力は「実質同一」範囲に広がりを有するが、その広がりは延長登録の枠組みとの整合性によって制約されるという基本構造を示した。
イ.複数延長がある場合の効力制限
本件では、同一特許について先後承認処分という複数の延長登録が存在する点が問題となった。この点について裁判所は、次のように踏み込んだ判断を示した。
「医薬品に係る同一の特許権について、複数の政令処分を理由とする延長登録がされている場合、後れて延長登録された特許権の効力範囲は、・・・一定の広がりを有するものではあるものの、少なくとも、先行する延長登録の理由となった政令処分の対象とする物と成分、分量、用法、用量、効能及び効果として同一の物は、後行する延長登録の理由となった政令処分の対象とする物と実質同一ではなく、その生産・譲渡等にまでは効力が及ばないものとして解されるべきである」
すなわち裁判所は、後行承認処分での延長の効力は、先行承認処分での延長の対象医薬品と同一の医薬品には及ばないと明確に判示した。
その理由についても、制度趣旨に基づき次のように説明する。
「仮に、後れて延長登録された特許権の効力が、・・・先行する延長登録の理由となった政令処分の対象とする物と成分、分量、用法、用量、効能及び効果として同一の物の生産・譲渡等にまで及ぶとすれば、先行する存続期間の延長の方が短かった場合において、その対象とする物の第三者による実施が、存続期間延長制度が規律する以上の期間にわたって禁じられることになる。」
さらに、第三者の予測可能性の観点からも次のように指摘する。
「既に延長期間が終了した延長登録の理由となった政令処分の対象とする物と成分、分量、用法、用量、効能及び効果として同一の物に対して特許権の行使を受けるということは、第三者の予期を期待できるものではなく、特許権の効力を及ぼす実質的正当性に欠けるものともいえる。」
以上より、本判決は、複数延長の場面においては「後行延長による再独占」を否定する明確な制限を課したものといえる。
ウ.本件への当てはめ
以上の法理を前提として、裁判所は、本件における被告製品と各延長登録との関係を検討した。
原告らは、本件12μg処分に基づく後行延長(本件延長登録1-2)の効力が、分量を24μgとする被告製品にも及ぶと主張した。
この点について裁判所も、原告製品12μgと被告製品(24μg)との関係について、分量差にとどまることから、形式的には「実質同一」と評価し得る余地があること自体は否定しなかった。
しかしながら、裁判所は次のとおり判示し、効力の及ぶ範囲を明確に限定した。
「被告製品は、まさに先行する本件延長登録1-1の理由とされた本件24μg処分の対象となった原告製品24μgと成分、分量、用法、用量、効能及び効果が同一の物であるところ、上記延長登録に係る延長期間は既に終了したものである。後行する本件延長登録1-2によって存続期間を延長された本件特許権1の効力は、その延長登録の理由となった本件12μg処分の対象である原告製品12μgと分量のみを異にする医薬品を実質同一の範囲に含むものとして一定の広がりを有するとまではいえるものの、・・・原告製品24μgとの同一性に係る上記一事をもって、少なくとも、被告製品は原告製品12μgと実質同一ではなく、その生産・譲渡等にまで効力は及ばないというべきである(被告製品と原告製品24μgとの間で、仮に添加剤の違いがあり、これをもって「成分」に一定の差異があると評価されるのであれば、実質同一をより否定する要素といえる。)。」
さらに裁判所は、原告の主張を採用した場合の帰結についても、次のように指摘した。
「仮に原告及び補助参加人の主張を認めた場合、・・・本件延長登録1-2によって存続期間が延長された本件特許権1の効力として、さらに令和10年12月26日までの間、被告製品その他原告製品24μgと成分、分量、用法、用量、効能及び効果を同じくする物の第三者による生産・譲渡等を差し止めることができることになる。これは、本来、政令処分を受けるまでの失われた期間に限り、存続期間の延長を許容する存続期間延長制度の趣旨、想定とは異なり、失われた期間の回復を超えて、延長登録の理由となった政令処分の対象とする物についての実施権の専有を認めるに等しく、実質において、特許権者と第三者との衡平を損なう結果を招くものといえる。」
また、ベバシズマブ最高裁判決の原判決であるベバシズマブ知財高裁判決の
「なお、政令で定める処分を受けることによって禁止が解除された特許発明の実施が、先行処分に基づき存続期間が延長された当該特許権の効力が及ぶ特許発明の実施の範囲に含まれるような場合は、重複して延長の効果が生じ得ることとなる。後行処分による延長期間が先行処分による延長期間より長い場合には、これに対応する期間、当該特許権の存続期間が延長されるが、当該期間については、当該特許発明の実施が禁止されていた部分があることに照らすと、上記のように解することに何ら不合理な点はない。」
との説示部分を引用した原告の主張に対して、裁判所は、以下のとおり重複して延長の効果が生じ得ることは認めた。
「上記説示部分が傍論であることをおくとしても、・・・先行する政令処分によって存続期間が延長された特許権の効力範囲が、後行する政令処分の対象とする物と同一の物の生産・譲渡等に及び得ること、そのように解したとして特段不合理な点はないということを述べるものである。すなわち、先行する政令処分とこれに基づく延長登録の際には、まだ後行の延長登録がされているわけではなく、延長登録の並列状態及びこれに伴う効力範囲の制約がない中で延長登録がされることになるため、後行する政令処分の対象とする物と同一の物の生産・譲渡等を包含するように効力範囲が及ぶ可能性があるといえる。」
しかし、裁判所は、これと逆の方向性、つまり後行承認処分によって存続期間が延長された特許権の効力範囲が、先行する承認処分の対象とする物と同一の物の生産・譲渡等にまで及び得るかについては、オキサリプラチン知財高裁判決やベバシズマブ知財高裁判決の趣旨を理解すると、一方向への片面的な包含関係はあり得ても、双方向に、つまり、「互いに実質同一の範囲に含まれる」ような効力範囲の解釈は否定されるべきであるとして、原告の主張を退けた。
「上記説示部分は何ら言及するものではなく、実際上も利害状況が大きく相違する。すなわち、後行する延長登録の際には、先行する延長登録(少なくとも、その出願)が存在するのであって、・・・後行する延長登録によって存続期間が延長された特許権の効力範囲につき、先行する延長登録との整合性を考慮して解釈しなければ、延長登録制度全体の趣旨を損ねることになるところ、少なくとも、先行する政令処分の対象とする物と成分、分量、用法、用量、効能及び効果が同一の物の生産・譲渡等にまで効力は及ばないものと解される。」
以上より裁判所は、後行延長の効力は、先行延長の対象であった24μg製剤(被告製品)には及ばないと結論付けた。
4.コメント
本判決は、医薬品特許の存続期間延長制度に関する近時の判決例の流れの中で、複数の延長登録が存在する場合における延長特許権の効力範囲の限界を明確に示した点で注目される。とりわけ本件は、侵害の成否が「技術的範囲」ではなく「延長特許権の効力範囲」によって決着した事案であり、特許権侵害判断と延長制度との関係が端的に表れたものといえる。
(1)技術的範囲と延長特許権効力の二段階構造
裁判所は、被告製品が本件発明の技術的範囲に属すること自体は肯定している。
本判決は、医薬用途発明に係る特許権の侵害判断に関し、被告が主張したいわゆる「ラベル論」や「専ら論」といった形式的な枠組みに依拠するのではなく、あくまで特許発明の構成要件の解釈を出発点として、被告製品の実施が当該用途発明の一態様としての実施に該当するかという観点から技術的範囲への属否を判断するという、特許法の原則に忠実な手法を採用している。すなわち、添付文書の記載を形式的に基準とするのではなく、用途発明としての技術内容への該当性を実質的に評価する姿勢が明確に示されている。
しかし、通常の特許権侵害判断の枠組みで見れば侵害が成立している関係にもかかわらず、最終的に侵害を否定したのは、上述したとおり、延長特許権の効力が当該製品に及ばないと判断したためである。
(2)延長特許権効力の広がりとその制度的制約
本判決は、延長特許権の効力が承認医薬品と形式的に同一の範囲に限定されるものではなく、「実質同一」と評価される範囲にまで広がり得るとするオキサリプラチン知財高裁判決(2017.01.22ブログ記事「2017.01.20 「デビオファーム v. 東和薬品」 知財高裁平成28年(ネ)10046」参照)の流れと整合する。「実質同一」であるか否かは、「特許発明の内容に基づき、その内容との関連で、政令処分において定められた「成分、分量、用法、用量、効能及び効果」によって特定された「物」と対象製品との技術的特徴及び作用効果の同一性を比較検討して、当業者の技術常識を踏まえて判断すべきと解される」点も再確認している。
そして、延長登録の単位と効力範囲とは同一ではなく、効力範囲の方が広がりをもった範囲を有することを改めて確認した。すなわち、延長登録要件と延長特許権の効力範囲を連動させる、いわゆる「連動論」の考え方を採用していない。
しかしながら、本判決の特徴は、この効力範囲となる実質同一の広がりを無限定のものとして捉えるのではなく、延長制度全体の整合性の中で「特許権者と第三者の衡平」の観点から明確な制約を課した点にある。すなわち、延長特許権の効力は実質同一の範囲に及び得るとしても、その広がりは延長登録の範囲・単位と抵触しないという制約の中で解釈されるべきであることを強調した。
そして本判決の核心は、この制約が複数延長の場面においてどのように具体化されるかを示した点にある。裁判所は、後行延長の効力が一定の広がりを持ち得ること自体は否定しないものの、先行延長の対象医薬品と同一の医薬品にまでその効力が及ぶことはないと判示した。
その理由として示されたのは、すでに延長期間が終了した医薬品について再度特許権の効力を及ぼすことは、特許権者と第三者との衡平を調整しようとする存続期間延長制度の趣旨を大きく損なうものであるとともに、第三者の予測可能性を害すること、さらに実質的正当性に欠けることにある。これらはいずれも、延長制度の根本的な趣旨に立ち返った説明であり、本判決が単なる事案処理にとどまらず、制度論としての整理を意識していることがうかがえる。
(3)非遡及的一方向性と延長制度の構造的限界
以上を踏まえると、本判決が示したルールは、延長特許権の効力に関する「非遡及的一方向性」として整理することができる。すなわち、先に存在する延長はその後の領域に影響を及ぼし得るとしても、後からの延長は過去に遡って効力を及ぼすことはできない。
本件に即していえば、先行する24μg製剤に係る延長は、場合によっては12μg製剤との関係でも実質同一の範囲として効力が及び得る。なぜなら本件各特許発明の内容に基づき、その内容との関連で、原告製品12μgと被告製品(24μg)との技術的特徴及び作用効果の合一性を比較検討すれば、「分量」という差異は僅かな差異又は全体的にみて形式的な差異にすぎないだろうからである。
一方で、後行する原告製品12μgに係る延長が、既に延長期間の満了した24μg製剤にまで及ぶことは否定される。この非対称的な関係は、延長特許の効力が時間軸に沿って一方向にのみ作用することを意味している。
このルールは、より端的には、「後から得た延長によって、既に自由となった領域を取り戻すことはできない」と表現することができる。そしてこのルールの背後にあるのは、一度、禁止が解除された処分についての補償期間が終わりパブリック・ドメインとなった技術利用は制限されるべきではないという要請と言い換えることができるかもしれない。
本判決は、複数延長という場面においてこの点を明確に示し、延長特許権の効力が有する構造的限界を具体的に画定したものといえる。
以上を総合すると、本判決は、延長特許権の効力について、実質同一の範囲への広がりを前提としつつも、その広がりが非遡及的にのみ認められること、すなわち既に自由となった領域に対する再度の独占を否定するという原則を明確にした点において、延長特許権の効力を判断した事案の中に新たな輪郭線を引いたものと評価することができる。
(4)本事件周辺の動き
本件をめぐっては、訴訟・審判の双方において複数の関連手続が並行して進行しており、その全体像を把握する上でこれらの動向も重要である。
まず、Viatris Inc.が2026年2月26日に提出した年次報告書(Form 10-K )によれば、2026年2月6日、大阪地方裁判所はヴィアトリス製薬による特許権侵害差止仮処分命令申立て(大阪地裁令和7年(ヨ)第20008号、同第20009号)を却下したが、同社はこれを不服として知的財産高等裁判所に控訴しているとされる。
また、アミティーザ®に関する特許権の範囲について、ヴィアトリス製薬が公衆及び厚生労働省に対して行った情報発信が不正競争行為に該当するとして、沢井製薬がその差止めを求めた別件訴訟においては、2025年12月、東京地方裁判所が請求を棄却し、当該事件は終結している。公衆への情報発信とは日刊薬業における謹告文掲載を指すものと解される(2023.03.15ブログ記事「ルビプロストンに関する特許権について」参照)。なお、この種の情報提供行為の適法性については、いわゆるアイリーア事件やリバーロキサバン事件が参考になる(2026.01.26ブログ記事「パテントリンケージにおける特許権者の情報提供は不競法違反か ― アイリーア®事件・知財高裁抗告棄却決定の確定」及び2025.12.17ブログ記事「2025.10.29「日本ジェネリック v. バイエル薬品」 東京地裁令和7年(ワ)70139 ― パテントリンケージ下の情報提供・謹告掲載と不競法上の信用棄損行為該当性」(『医薬系特許的判例ブログ年報 2025』 Fubuki著 2026年3月発行, p272-282)参照)。
さらに、特許無効の観点からの攻防も活発である。2023年9月以降、沢井製薬は、特許第4332353号(本件特許2)及びアミティーザ®カプセル12µgの承認に基づく同特許の存続期間延長登録について、無効審判(無効2023-800077号及び無効2023-800063号)を請求したが、2025年4月及び同年6月に、いずれも特許及び延長登録の有効性を維持する審決がなされている。これに対し、沢井製薬は審決取消訴訟(令和7年(行ケ)第10055号及び同第10064号)を提起しており、現在も係争中である(このうち、令和7年(行ケ)第10064号については、2026年4月9日に判決の言渡しが予定されている)。
なお、同24µgの承認に基づく同特許の存続期間延長登録についても、沢井製薬が請求した無効審判(無効2023-800062号)に係る請求不成立審決の取消訴訟(令和7年(行ケ)第10059号)が提起され、2026年4月9日に判決の言渡しが予定されている。ただし、当該訴訟の帰趨は、12µg承認処分に基づく延長特許権の効力を直接の争点とする本件の結論に影響を及ぼすものではないと解される。
また、特許第4889219号(本件特許1)についても、同12µgの承認に基づく存続期間延長登録に関し、沢井製薬及び東和薬品がそれぞれ無効審判(無効2024-800052号及び無効2025-800139号)を請求しており、こちらについても係争が継続している。
加えて、2024年4月以降、沢井製薬は、2025年10月、2026年9月、2027年8月、2027年11月及び2028年12月にそれぞれ満了する複数の特許について、原告製品12µgに係る存続期間延長登録の無効審判を順次請求するとともに、2027年8月満了の特許自体についても無効審判を請求している。このうち、2026年1月には、特許庁が当該特許の有効性を維持する旨の判断を示している(2023.03.15ブログ記事「ルビプロストンに関する特許権について」参照)。
パテントリンケージの運用が本件においてどのように行われたのかも、重要な関心事項である。本件各発明は用途特許としてパテントリンケージの対象に含まれるところ、被告製品は本判決言渡し(2026年3月3日)前である同年2月16日に既に承認されている。すなわち、厚生労働省は、本案判決を待つことなく、仮処分命令申立事件(大阪地裁令和7年(ヨ)第20008号、同第20009号)の却下決定(同月6日)後に、延長された特許権の効力が被告製品に及ぶか否かを独自に判断したことになる。
もっとも、その判断過程は公表されておらず、試行導入された専門委員制度が本件で活用されたか否かも明らかではない(2025.11.25ブログ記事「厚労省、パテントリンケージの運用に専⾨委員制度を試行的に導⼊」(『医薬系特許的判例ブログ年報 2025』 Fubuki著 2026年3月発行, p283-287)参照)。結果としては、被告製品の製造販売が特許権を侵害しないとの点で、本判決と行政判断は整合しており、実務上の齟齬は顕在化していないともいえる。

しかしながら、本件のように判例上の明確な規範が未形成の領域において、行政が先行して非公開のロジックに基づきパテントリンケージの解除判断を行っているとすれば、その透明性や予見可能性の観点からはなお課題が残る。本件においては、仮処分段階の判断と本案判決が結果的に一致したものの、過去には仮処分と本案で結論が分かれた事例も存在する(2023.11.29ブログ記事「2023.11.29ブログ記事「BMS スプリセル®錠(一般名:ダサチニブ水和物)の後発品を巡る特許権侵害訴訟で東京地裁が沢井製薬のダサチニブ錠の製造販売行為を禁止する仮処分命令を発出 ― 本当の問題点 ―」及び2025.06.24ブログ記事「2025.05.15 「沢井製薬 v. BMS」 東京地裁令和5年(ワ)70527・令和6年(ワ)70016 ― スプリセル®後発品訴訟で特許権延長制度の根幹を揺るがす形式判断」(『医薬系特許的判例ブログ年報 2025』 Fubuki著 2026年3月発行, p126-135)参照)。
このような状況のもとでは、当事者のみならず他の後発医薬品メーカーにとっても、どのような基準により特許権の効力が行政内部で評価されるのかが見えにくい。制度運用としての安定性を確保する観点からも、承認審査過程の一定の可視化など、厚生労働省側の判断過程の透明化に向けた制度設計が求められるところである(田村善之「パテント・リンケージ制度について」「医薬系”特許的”判例」ブログ 2026年3月19日記事参照)。

以上のとおり、本件をめぐる紛争は、侵害訴訟、仮処分、情報発信をめぐる不正競争訴訟、延長登録及び特許自体の有効性を争う審判・審決取消訴訟、さらにはパテントリンケージという制度面の問題にまで広がっており、多層的かつ長期的な係争構造を形成している点に特徴がある。
この点に関連して、被告である沢井製薬は、本判決言渡日と同日の2026年3月3日、同年2月に製造販売承認を取得した被告製品(ルビプロストンカプセル24μg「サワイ」)について、薬価収載に支障は生じない旨を公表している。他方で、その具体的な収載時期については未定とされている(2026.03.03 沢井製薬 press release: ルビプロストンカプセル24μg「サワイ」特許権侵害差止請求事件に関する勝訴のお知らせ)。このように、行政判断・司法判断・市場導入の各プロセスが必ずしも同期して進行するわけではない現状も踏まえると、本件は、延長特許権の効力論にとどまらず、パテントリンケージ制度の運用の在り方を改めて問い直す契機となる事例であるといえよう。
※ご覧いただきありがとうございます。この記事の内容について、読者の皆さまのご意見や気づきもぜひお聞かせください!
以下のようなご感想・質問、大歓迎です!
- 🤔ここ理解しづらいな、という部分はありましたか?
- 🤔このニュース、事件、判決例の実務影響についてご意見ありますか?
- 🤔過去の類似事例や判決例をご存じでしたら教えてください!
- 🤔恥ずかしい質問、つぶやき、大歓迎です
- 「👍」「なるほど」「疑問あり」だけでもOK!
コメント欄は↓ コメントは匿名OK! ぜひ気軽に投稿してください🙇
皆さんの反応が、次回の記事や解説のヒントになります🥰
Robot icons created by Freepik – Flaticon; Robot cat icons created by Freepik – Flaticon





コメント
丁寧な分析拝見いたしました。一点気になったのが、先行医薬品に効力が及ぶかどうかってそんなに大事な問題なんですかね?普通の場合は添加物が違うので先行医薬品そのものが除かれてもあまり関係がないように思います。その点謎なのが、今回の場合は、アミティーザ12mcgと後発品は成分分量用法用量効能効果が同じらしいですね。本当にそんなことがあるんだろうか、という気がしています。
ご意見ありがとうございます。
ご指摘のとおり、通常は添加物の違いなどにより、先行医薬品そのものと後発医薬品が完全に一致する場面は多くはなく、「そのもの」が効力範囲から外れるとしても、直ちに実務上大きな問題にならないケースも少なくないと思われます。
もっとも、本件でさらに想起される疑問は、まさにその「そのものが除かれる」という判断の先にある射程です。すなわち、仮に先行医薬品そのもの(同一の後発医薬品)には効力が及ばないとすると、では先行医薬品と「実質同一」と評価される範囲のものについてはどのように扱われるのか、という点が問題となります。
例えば、ご指摘のように、仮に後発医薬品24μgにおいて添加物の一部が異なっていた場合、それは「同一」ではないが「実質同一」と評価され得る場面が想定されます。このとき、先行医薬品(と同一の後発医薬品)には効力が及ばないとしつつ、その周辺に位置する「実質同一」の製品には効力が及ぶのか、それとも同様に除外されるのかという線引きが問題となります。
さらに、承認対象(いわゆる5要件)や特許発明の内容との関係によっても、同一・実質同一の評価は様々なバリエーションがあり得ます。そのため、単に「そのものが除かれるか」という点にとどまらず、先行と後行の関係の中で、どこまで効力が及び、どこから及ばないのかという範囲設定の問題として、本件は一定の意義を有すると考えています。
また、ご指摘のとおり、本件のように成分・分量・用法・用量・効能効果が一致するという事例はやや特異にも見え、その点も含めて興味深い事案であると感じております。
ありがとうございます。確かにこの判決が残した問題もまだ沢山あるのかな、と思います(それこそ判決が言うような先行延長出願していないケースなど)。もし実質同一物をまるごと効力範囲から除くということになると延長特許の効力範囲の重なりを認めないことになり、これまでの裁判例とは考え方を大きく変える(連動論復活?)しかなさそうです。控訴審も進んでいると思いますのでそちらの判決が期待されますね。