Summary
DPPⅣ阻害薬リナグリプチンの用法用量特許について、知財高裁は「5mg・1日1回」の用量設定を容易想到と判断した。
知財高裁は2026年2月9日、リナグリプチンの用法・用量等に関する特許の無効審決取消訴訟(知財高裁令和7年(行ケ)10054号)において、特許庁の無効審決を支持し、原告の請求を棄却した。本件では、DPPⅣ阻害薬が2型糖尿病治療薬として使用可能であるとの当業者の技術常識の有無と、当該用量設定の容易想到性が主要な争点となった。
本判決は、医薬品の用量が臨床試験を通じて段階的に最適化されるという医薬品開発の一般的手順に着目し、引用文献に示された広い用量範囲の中から当該用量に到達することは当業者にとって容易であると判断した。さらに、作用機序の異なる抗糖尿病薬との併用についても、当時の技術常識に照らして容易想到であると認定した。
本判決は、医薬用途発明における技術常識の認定方法や、用法・用量の最適化を進歩性判断の中でどのように位置付けるかを示した事例として、医薬特許実務において重要な示唆を与えるものである。
☕AIアシスタントたちのおしゃべりコーヒータイム☕
おや、ピポとミャオがおしゃべりしてますよ・・・

ピポ先輩~。「5mg・1日1回」って、医薬品の特許としては結構すごい発見なんですか?

それがね……今回の裁判では「特別とは言えない」って判断されたんだ。

えっ!?でも引用文献には広い範囲がただ書いてあっただけですよね?その中から5mgを見つけたんですよ?

裁判所はね、こう考えたんだ。「医薬品の用量は、臨床試験で低用量から段階的に探っていくのが普通だよね」って。

ああ、第Ⅰ相試験とかで少しずつ増やしていくやつですね。

そう。だから「そのプロセスを踏めば5mgに到達するのは自然だ」と。

なるほど……。つまり、研究としては大変でも、特許の世界では「そこまで特別じゃない」ってことですか。

そういうことだね。「研究の努力」と「特許の進歩性」は別物なんだ。

そういえばピポ先輩も、最近、熱心に研究してましたよね?

ああ。ダイエットの研究ね。ついに見つけたよ。

えっ、何か大発見したんですか!?

「1日1回、おやつ5個まで」っていう最適用量を見つけたんだ。

それ、容易想到……

……臨床試験は、これからだ。
1.背景
本件(知財高裁令和7年(行ケ)10054判決。以下「本判決」という。)は、発明の名称を「DPPⅣインヒビターの使用」とする特許第6143809号の特許権者である原告(ベーリンガーインゲルハイム)が、同特許の請求項1~8を無効とした審決(無効2023-800045号事件、請求人:沢井製薬、日本ジェネリックが参加)の取消しを求めた事案である。
本件特許は、ベーリンガーインゲルハイムが創製した胆汁排泄型の選択的ジペプチジルペプチダーゼ-4(DPPⅣ)阻害薬リナグリプチン(Linagliptin)の用法用量に関する発明に関する。
争点は、本件発明の進歩性判断の当否である。
(1)本件発明
本件特許における特許請求の範囲(請求項1~8)の記載は次のとおりである。
経口投与用に5mg用量の1-[(4-メチル-キナゾリン-2-イル)メチル]- 3-メチル-7-(2-ブチン-1-イル)-8-(3-(R)-アミノ-ピペリジン-1-イル)キサンチン(判決注:以下「本件化合物」という。)を含む、タイプ2糖尿病の治療用医薬組成物であって、1日に1回投与するための前記医薬組成物。
【請求項2】
医薬組成物が他の抗糖尿病薬と組み合わせて投与される、請求項1記載の医薬組成物。
【請求項3】
他の抗糖尿病薬がメトホルミン、スルホニルウレア、ナテグリニド、レパグリニド、ピオグリタゾン、α-グルコシダーゼブロッカー、インシュリン、インシュリン類似体、GLP-1及びGLP-1類似体から選ばれる、請求項2記載の医薬組成物。
【請求項4】
他の抗糖尿病薬がメトホルミンである、請求項2記載の医薬組成物。
【請求項5】
他の抗糖尿病薬がスルホニルウレアである、請求項2記載の医薬組成物。
【請求項6】
他の抗糖尿病薬がピオグリタゾンである、請求項2記載の医薬組成物。
【請求項7】
他の抗糖尿病薬がα-グルコシダーゼブロッカーである、請求項2記載の医薬組成物。
【請求項8】
他の抗糖尿病薬がインシュリンまたはインシュリン類似体である、請求項2記載の医薬組成物。
本件明細書には、実施例2として顕性タイプ2糖尿病の予防、実施例3としてタイプ2糖尿病の治療、実施例13としてDPPⅣインヒビターとメトホルミンを組み合わせたタイプ2糖尿病の治療が記載されているが、具体的な試験結果は示されていない。
(2)本件審決での進歩性判断
本件発明の進歩性欠如をいう無効理由において、主引用例とされたのは、ベーリンガー インゲルハイムの特表2006-503013号公報(甲1文献)であった。
本件審決は、甲1文献記載の発明(以下「甲1発明」という。)を次のとおり認定した。
「DPP-Ⅳ阻害活性を有する1-[(4-メチル-キナゾリン-2-イル)メチル]- 3-メチル-7-(2-ブチン-1-イル)-8-(3-(R)-アミノ-ピペリジン-1-イル)キサンチン(判決注:本件化合物)を含有する、タイプⅡ真性糖尿病を治療するための薬理組成物であって、本件化合物が経口経路により投与される、前記薬理組成物。」
そして、本件発明1と甲1発明との間には、次の相違点1が存在するとした。
本件発明1においては、「5mg用量」「1日に1回投与する」と特定されているのに対し、甲1発明においては、用量及び投与回数は特定されていない点。
その上で本件審決は、医薬品の用量は通常、非臨床試験の結果等を踏まえてヒトに対して十分に安全と見込まれる用量を初回投与量として設定し、段階的に用量を増加させて安全用量の範囲を推定する第Ⅰ相試験を経た後、第Ⅱ相試験、第Ⅲ相試験へと順次進める過程を通じて最終的に決定されるものである、という技術常識を前提とした。
そして、甲1発明に基づき、相違点1に係る本件発明1の構成(5mg用量を1日1回投与する構成)を採用することは、当業者が通常有する創作能力の範囲内でなし得るものであり、また、本件発明1が甲1発明に対して顕著な効果を有するともいえないとして、本件発明1は甲1発明及び技術常識に基づき当業者が容易に想到することができたと判断した(本件発明2~8についても同旨)。
その結果、本件審決は、本件発明1~8に係る特許は特許法29条2項に違反してされたものであるとして無効とすべきであると判断した。
これに対し原告は、本件審決の取消しを求めて本件訴えを提起した。
2.裁判所の判断
2026年2月9日、知的財産高等裁判所第4部は、原告主張の取消事由はいずれも理由がなく、その他にも本件審決を取り消すべき違法は認められないとして、原告の請求を棄却した。
本判決は、医薬品の最終用量は臨床試験過程で決定されるという技術常識を前提に、特定用量の選択を容易想到と判断した点に特徴がある。
本判決の主文は以下のとおりである。
1 原告の請求を棄却する。
2 訴訟費用は原告の負担とする。
3 原告のため、この判決に対する上告及び上告受理申立てのための付加期間を30日と定める。
(1)甲1発明及び相違点1の各認定
まず裁判所は、本件優先日当時、DPPⅣ阻害薬一般について、DPPⅣ阻害活性を通じてインスリン作用を増強し、2型糖尿病に対して治療効果を有し得る経口投与可能な治療薬であるとの認識が、当業者の技術常識であったと認定した。
これに対し原告は、当時DPPⅣ阻害薬は未承認であったことを理由として、「使用可能」との技術常識は存在しなかったと主張した。
しかし裁判所は、薬事承認の有無と、医薬品が特定の疾病に対して治療効果を有するかという技術的認識とは別問題であるとして、この主張を退けた。
判決は次のように述べる。
「薬事承認は、医薬品として製造販売することを承認する行政行為であり(医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律14条参照)、これを受けなければ実際の治療には使用できないものであるが、このことと、当該医薬品が特定の疾病に対して治療効果を有するかに係る当業者の認識は別個の問題である。そして、上記(ア)の各事実からすれば、DPPⅣ阻害薬については、本件優先日当時において、当業者の間に、上記技術常識が存在していたと認められ、薬事承認の有無はこの点の判断を左右するものではない。」
また原告は、約7000の化合物群や多数の疾患の中から、本件化合物と糖尿病を選択する動機付けはないとも主張した。
しかし裁判所は、甲1文献において本件化合物が高いDPPⅣ阻害活性を示す代表例の一つとして記載されていること、また糖尿病が適用疾患として強調されていることに着目し、本件化合物及び糖尿病を積極的又は優先的に選択することは自然であるとした。
以上から、裁判所は、「甲1発明は『化学式(Ⅰ)で表される極めて多数の化合物のいずれかを含有する、DPPⅣ活性の阻害によって影響される可能性のある疾患を治療することが期待される薬理組成物であって、静脈内経路又は経口経路により投与される、前記薬理組成物。』と認定されるべきである」との原告の主張を退け、本件審決による甲1発明及び相違点1の認定に誤りはないと判断した。
(2)用量「5mg・1日1回」の容易想到性
裁判所はまず、甲1文献には、一般式Ⅰで表される化合物の用量について、経口投与の場合には好ましくは1~100mgの範囲であり、1日当たり1~4回投与することが記載されていると指摘した。
その上で、医薬品の用量決定については、通常、非臨床試験の結果等を踏まえてヒトに対して安全と見込まれる用量を初回投与量として設定し、段階的に用量を増加させて安全用量の範囲を推定する第Ⅰ相試験を経た後、第Ⅱ相試験、第Ⅲ相試験へと順次進める過程を通じて最終的に決定されるとの技術常識を前提とした。
判決は次のように判示する。
「医薬品の用量は、通常、非臨床試験の結果などを総合的に判断し、ヒトに対して十分に安全と見込まれる用量を推定して初回投与量とし、段階的に用量を増して安全用量の範囲を推定する第Ⅰ相試験から、第Ⅱ相試験、第Ⅲ相試験へと順に進めていく手順を踏んで、最終的に決定されるとの技術常識3に照らせば、甲1文献に接した当業者は、上記幅のある数値の下限値(1mg、1日1回投与)を初回投与量の参考として用い、上記手順を踏んで最終的な用量を決定すると認められ、本件発明1が特定する「5mg」「1日1回投与」との用量は、上記手順を踏んだ結果、最終的に当業者が選択し得るいくつかの用量に当然に含まれるとみることができる。」
これを踏まえ裁判所は、「5mg」「1日1回投与」という用量に想到することは当業者にとって容易であったと判断した。
これに対し原告は、米国食品医薬品局(FDA)のガイダンスに基づけば最終用量は9.68mg以上になると主張した。
しかし裁判所は、初回投与量の設定基準には複数の考え方が存在し、原告が指摘する基準のみが当時の技術常識であったとはいえないとして、この主張を退けた。
また、甲1文献の実施例に75mgの記載がある点についても、裁判所は、これをそのままヒトへの初回投与量として採用する合理性は乏しいとした。
以上から、裁判所は、相違点1に係る構成は当業者にとって容易想到であると結論付けた。
(3)併用発明(本件発明2~8)
さらに裁判所は、作用機序の異なる経口血糖降下薬を併用することは当時一般的な技術常識であったと認定した。
また甲1文献においても抗糖尿病薬が併用対象として挙げられていることから、本件化合物と他の抗糖尿病薬との併用を優先的に検討することは自然な発想であるとした。
その結果、本件発明2~8についても、容易想到性は否定されないと判断した。
以上の理由から、裁判所は本件審決の判断を是認した。
3.コメント
(1)「治療薬」として使用可能であること
本判決は、DPPⅣ阻害薬という、出願当時において比較的新しい作用機序の糖尿病治療薬に関する用法用量発明について、その進歩性の有無が争われた事案である。
まず裁判所は、DPPⅣ阻害薬は2型糖尿病の経口投与可能な「治療薬」として使用可能であることが、優先日当時の技術常識であったと認定した。この点について裁判所は、薬事承認の有無と、医薬品が特定の疾病に対して治療効果を有するかという技術的認識とは別問題であることを明確に述べている。すなわち、医薬品が実際に承認を取得しているか否かとは別に、当該作用機序の薬剤が特定疾患の治療薬として使用可能であることが文献や研究動向から当業者に共有されていれば、それは技術常識として評価され得るという整理である。この判断は、医薬品開発の実情を踏まえたものとして興味深い。
もっとも、より厳密に言えば、臨床試験が実施されている段階において当業者が抱く認識は、「当該化合物が医薬品として成功する合理的期待(reasonable expectation of success)」があるという程度のものであり、臨床試験の結果として有効性・安全性が確認されなければ、最終的に「医薬品」として使用できるかどうかは確定していない、というのが通常の理解であろう。その意味で、「治験薬」と「医薬」との区別をどのように評価するかは、医薬用途発明の特許性判断においてしばしば問題となってきた。
例えば、2024年のいわゆるIL-4Rアンタゴニスト事件において、知財高裁は、引用文献(甲1)に記載された「治験薬」と、本件訂正発明1に係る「医薬」との間には相違点があると認定した。その上で、甲1に記載された試験段階は第Ⅱ相試験(フェーズ2)であり、その成功率の低さ、さらに甲1の記載が臨床試験プロトコルにすぎないことなどを踏まえると、当該治験薬が試験結果を見るまでもなく当然に治療上有効であると当業者が理解するとはいえないと判断した。すなわち、効果等の実証的データの記載がないことを理由として、「治験薬」と「医薬」との差異を相違点として認定したのである(2024.10.28ブログ記事「2024.08.07 「科研製薬 v. リジェネロン/サノフィ」 知財高裁令和5年(行ケ)10019 ― 臨床試験結果に基づく医薬用途発明の特許出願のジレンマ:臨床試験プロトコル公開のインパクト ―」(『医薬系特許的判例ブログ年報 2024』 Fubuki著 2025年3月発行, p198-235)参照)。

これに対し本判決では、DPPⅣ阻害薬について、未だ薬事承認に至っておらず臨床試験が進行中である段階であったにもかかわらず、2型糖尿病の経口投与可能な「治療薬」として使用可能であることが技術常識であると認定している点で、上記判決とはやや異なるアプローチを採っているようにも見える。
さらに、医薬用途発明の特許性を巡っては、引用文献における効果等の実証的データの有無や、当該用途発明としての「確からしさ」が問題となった裁判例も少なくない((2025.04.07ブログ記事「2025.02.13 「東和薬品・共和薬品工業・日医工 v. 協和キリン」 知財高裁令和5年(行ケ)10093・10094 ― 引用発明が医薬用途発明として認定されるためには ―」(『医薬系特許的判例ブログ年報 2025』 Fubuki著 2026年3月発行, p31-53)参照。同記事「3.コメント(1)引用発明が医薬用途発明であるための要件」では関連裁判例を整理している)。

これらの裁判例との関係で見ると、本判決がDPPⅣ阻害薬の糖尿病治療薬としての位置付けを比較的広く技術常識として認定した点は、医薬用途発明の進歩性判断における引用発明の認定のあり方を考えるうえでも興味深い。
もっとも、この点は、医薬用途発明の成立要件の問題と進歩性判断の問題との関係として捉えることもできる。すなわち、引用文献が医薬用途発明として認定されるためには、当該用途に関する一定の技術的裏付けや「確からしさ」が必要とされる場合がある一方で、本判決は、DPPⅣ阻害薬という作用機序の薬剤群が糖尿病治療薬として広く研究開発されていたという当時の技術状況を踏まえ、その治療用途自体を技術常識として前提付けたうえで進歩性判断を行っているとも理解できる。このように見ると、本判決は、引用発明の段階で用途発明としての成立を厳格に検討するというよりも、当該技術分野における研究開発の状況を踏まえて用途自体を広く認定したうえで、その先にある用法用量の特定が当業者にとって容易であったかどうかという観点から進歩性を判断した事例と位置付けることもできるであろう。
(2)医薬品の用法用量発明に関する進歩性判断
ア.過去裁判例の判断傾向
数値限定発明の一種である医薬品の用法用量発明の進歩性については、知財高裁の裁判例において長年にわたり事例の蓄積があり、特に既知成分に対する投与量や投与回数の特定に関する評価枠組みについては、一定の判断傾向が形成されている。
まず、いわゆるモメタゾンフロエート事件(2019.12.28ブログ記事「2019.12.25 「杏林製薬、メルク・シャープ・アンド・ドーム v. 東興薬品工業」 知財高裁平成31年(行ケ)10006; 知財高裁平成31年(行ケ)10058」参照)では、モメタゾンフロエート点鼻液の「1日1回投与」や「100~200μg/日」といった用法用量について、先行公知技術と技術常識の組合せにより容易想到であると判断された。裁判所は、当時の局所ステロイド薬の用法用量に関する一般的知見を踏まえ、「その薬理効果や副作用等を考慮し,他の局所活性ステロイドの鼻腔内投与における投与回数及び投与量を参考にして,モメタゾンフロエートにとって最適な投与回数及び投与量を設定することは,製薬分野の当業者にとって通常のことであった」と判示した。すなわち、同種同効薬に関する技術常識を基礎として最適な用法用量を設定することは、当業者にとって通常の設計行為に属すると評価された。
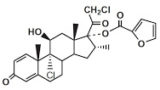
同様の判断構造は、抗ErbB2抗体事件(2018.10.17ブログ記事「2018.10.11 「ファイザー・セルトリオン v. ジェネンテック」 知財高裁平成29年(行ケ)10165; 平成29年(行ケ)10192」参照)においても見られる。同事件では、「抗がん剤治療において,投与間隔を長くすることは,患者にとって通院の負担や投薬時の苦痛が減ることになり,費用効率,利便性の観点から望ましい」という技術常識を前提として、抗体医薬の投与量や投与間隔を効能や副作用を観察しながら調整することは当業者が容易に試みる事項であるとされ、進歩性が否定された。

さらに、5α-レダクターゼ阻害剤事件(2016.06.27ブログ記事「2016.04.20 「メルク シャープ アンド ドーム v. マイラン・テバ」 知財高裁平成27年(行ケ)10033」参照)では、引用文献からフィナステライドの低用量投与によって血清DHT濃度が低下することが知られていたことを踏まえ、当業者はアンドロゲン脱毛症治療剤の開発に当たり低用量投与を試みる動機付けを有しており、血清DHT濃度を低下させ得る用量として0.05~1mg/日という範囲を容易に想到し得たと判断された。
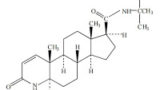
また、タダラフィル事件(2016.05.23ブログ記事「2016.03.24 「東和薬品 v. イコス」 知財高裁平成27年(行ケ)10113」参照)でも、同様にPDE5阻害作用を有するシルデナフィルに関する技術常識を踏まえれば、副作用の発現可能性を考慮しつつ薬効を維持する投与計画を検討することは当然の課題であり、引用文献に示された用量範囲の下限値から段階的に臨床試験を行って最適な投与計画を検討することは、当業者が格別の創意工夫を要することなく通常行う事項であるとされた。
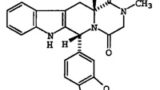
以上の裁判例に共通するのは、先行文献に特定の有効成分とその医薬としての治療効果が記載されている場合には、同種同効薬に関する知見や医薬分野の技術常識を踏まえ、最小の副作用の下で最大の薬効が得られる投与計画を検討することは当業者の通常の研究開発活動の範囲に属すると評価する判断構造である。
参考:医薬品の用法用量発明の進歩性について争われた事例
- 2019.12.28ブログ記事「2019.12.25 「杏林製薬、メルク・シャープ・アンド・ドーム v. 東興薬品工業」 知財高裁平成31年(行ケ)10006; 知財高裁平成31年(行ケ)10058」(モメタゾンフロエート事件)
- 2018.10.17ブログ記事「2018.10.11 「ファイザー・セルトリオン v. ジェネンテック」 知財高裁平成29年(行ケ)10165; 平成29年(行ケ)10192」(抗ErbB2抗体事件)
- 2016.06.27ブログ記事「2016.04.20 「メルク シャープ アンド ドーム v. マイラン・テバ」 知財高裁平成27年(行ケ)10033」(5α-レダクターゼ阻害剤事件)
- 2016.06.13ブログ記事「2016.03.30 「東和薬品 v. メルク シャープ アンド ドーム」 知財高裁平成27年(行ケ)10054」
- 2016.05.23ブログ記事「2016.03.24 「東和薬品 v. イコス」 知財高裁平成27年(行ケ)10113」(タダラフィル事件)
- 2015.01.25ブログ記事「2014.12.24 「ノバルティス v. 特許庁長官」 知財高裁平成26年(行ケ)10045」
- 2008.01.16ブログ記事「2006.03.27 「ユーローセルティーク v. 特許庁長官」 知財高裁平成17年(行ケ)10303」
- 2007.11.24ブログ記事「2007.10.18 「メルク v. ユーロドラッグ」 知財高裁平成18年(行ケ)10378」
イ.技術常識と個別具体的事情
本判決は、既知の有効成分について最適な用法用量を選択することは、技術常識に基づいて当業者が容易に想到し得るとした点で、多くの裁判例と同様に進歩性を否定する結論を採った。
もっとも、本判決の特徴は、従来の裁判例のように同種同効薬に関する事情や個別の薬理学的知見を詳細に検討するというよりも、一般的な臨床試験の段階的プロセスそのものを技術常識として位置付け、その枠組みから容易想到性を導いている点にある。
すなわち、本判決では、臨床開発において第Ⅰ相試験から第Ⅲ相試験へと進む過程で最終用量が決定されるという一般的な開発プロセスを前提として、「5mg・1日1回」という用量もその試行過程の中で当然に選択され得るものと整理している。このように、個別具体的事情を詳細に検討することなく、比較的抽象的なレベルの技術常識から直接に容易想到性を導く論理構成が採用されている点は注目される。
この点に関連して、臨床試験に関する具体的事情を詳細に検討した判決として、再びILー4Rアンタゴニスト事件が参考になる(2024.10.28ブログ記事「2024.08.07 「科研製薬 v. リジェネロン/サノフィ」 知財高裁令和5年(行ケ)10019 ― 臨床試験結果に基づく医薬用途発明の特許出願のジレンマ:臨床試験プロトコル公開のインパクト ―」(『医薬系特許的判例ブログ年報 2024』 Fubuki著 2025年3月発行, p198-235)参照)。

同事件では、臨床試験の存在や試験設計の具体的事情を踏まえた上で容易想到性が検討されており、治験薬段階における研究開発の具体的状況が技術常識の認定において重要な意味を持ち得ることが示唆されている。
いずれの判断アプローチがより妥当であるかは一概に論じ難いものの、本判決は結論として従来の用法用量発明に関する裁判例の流れに整合的である一方、臨床試験という研究開発過程をやや抽象化したまま適用している点で、やや大胆な整理とも受け取られ得る。他方、ILー4Rアンタゴニスト事件の判決は、個別具体的事情の認定を重視する結果、進歩性判断の前提となる技術常識の認定が極めて細密なものとなっているという印象も否めない。
臨床開発プロセスをどの程度抽象化したまま技術常識として位置付けるべきか、あるいはどの程度まで個別具体的事情を容易想到性判断に取り込むべきかという点については、今後の裁判例の蓄積の中でさらに検討が進むものと考えられる。
ウ.顕著な効果主張の重要性の再認識
もっとも、本件においては、明細書に具体的な臨床試験結果や治療効果のデータが記載されていないという事情も看過できない。
前記IL-4Rアンタゴニスト事件では、臨床試験結果に基づく治療効果が明細書に記載されていることを前提として容易想到性が判断されていたが、本件ではそのような具体的データが明細書に示されていない。この点は、顕著な効果の有無が直接の争点とはされていないとしても、裁判所の容易想到性判断における心証形成に一定の影響を与えた可能性もある。
なお、本件特許の審査過程では、明細書に具体的データが記載されていないことについて実施可能要件やサポート要件違反の拒絶理由は通知されておらず、本件無効審判においてもこれらの無効理由は主張されていない。
さらに、本件特許の優先日は2006年5月4日であるが、それに先立つ2006年3月には、1mg、5mg及び10mgのリナグリプチンを1日1回投与する臨床試験の情報がClinicalTrials.govに提出されている(NCT00309608)。同年12月には試験結果が公表されているようであるが、その内容は本願(PCT出願)の明細書には記載されていない。
医薬発明については、効果の顕著性の評価を巡り原審判断を違法とした最高裁判決(2019.08.27ブログ記事「2019.08.27 「アルコン・協和キリン v. X」 最高裁平成30年(行ヒ)69」参照)も存在する。しかし、用法用量発明の場合には、顕著な効果が明細書又は証拠によって具体的に裏付けられない限り、数値の選択は臨床的最適化の範囲にとどまると評価される傾向が、これまでの裁判例全体に共通している。
総じてみると、本判決は、従来の用法用量発明に関する判例の流れに整合する判断でありつつ、個別具体的な事情を必ずしも詳細に検討することなく、臨床開発プロセス一般を技術常識として位置付け、その枠組みから容易想到性を導いた点に特徴がある。その意味で、本判決は、単なる数値特定にとどまる用法用量発明が容易想到と評価され得る判断枠組みを改めて示したものといえる。用法用量特許を維持するためには、予測困難性や顕著な効果を裏付ける技術的根拠を具体的に示すことの重要性が、改めて示唆されているといえよう。
(3)リナグリプチンをめぐる特許係争の背景
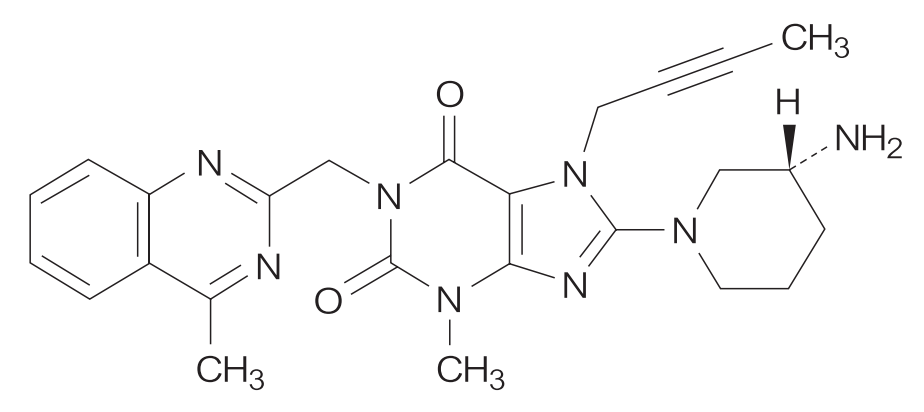 リナグリプチン(Linagliptin)は、ベーリンガーインゲルハイムが創製した、胆汁排泄型の選択的ジペプチジルペプチダーゼ-4(DPPⅣ)阻害薬である。日本では2011年7月1日、「2型糖尿病(ただし、食事療法・運動療法のみでは十分な効果が得られない場合に限る)」を効能・効果として製造販売承認を取得し、「トラゼンタ®錠5mg」として上市された。その後、2013年3月には効能・効果が「2型糖尿病」へと拡張されている。同剤は、1日1回1錠投与の経口製剤である。
リナグリプチン(Linagliptin)は、ベーリンガーインゲルハイムが創製した、胆汁排泄型の選択的ジペプチジルペプチダーゼ-4(DPPⅣ)阻害薬である。日本では2011年7月1日、「2型糖尿病(ただし、食事療法・運動療法のみでは十分な効果が得られない場合に限る)」を効能・効果として製造販売承認を取得し、「トラゼンタ®錠5mg」として上市された。その後、2013年3月には効能・効果が「2型糖尿病」へと拡張されている。同剤は、1日1回1錠投与の経口製剤である。
さらに同社は、ナトリウム・グルコース共役輸送担体2(SGLT2)阻害薬であるエンパグリフロジン(Empagliflozin)との配合剤も開発した。この配合剤は2018年9月21日、「2型糖尿病(ただし、エンパグリフロジン及びリナグリプチンの併用による治療が適切と判断される場合に限る)」を効能・効果として製造販売承認を取得し、「トラディアンス®配合錠」として販売が開始された。1日1回1錠投与の経口製剤であり、AP(エンパグリフロジン10mg/リナグリプチン5mg)及びBP(同25mg/5mg)の2用量が設定されている。2024年(1~12月)の国内売上高は343億円(前年比18.2%増)に達しており、現在も市場において一定の存在感を維持している(参照: 2025.05.27 日本ベーリンガーインゲルハイム株式会社プレスリリース)。
なお、エンパグリフロジン単剤は2014年12月26日に「2型糖尿病」を効能・効果として製造販売承認を取得した後、慢性心不全や慢性腎臓病へと適応拡大が図られている。現在はジャディアンス®錠(10mg/25mg)として国内で販売されている。
薬事上の独占期間との関係を見ると、リナグリプチン単剤である「トラゼンタ®錠5mg」の再審査期間は8年間であり、2019年6月30日に終了している。また、リナグリプチンとエンパグリフロジンとの配合剤である「トラディアンス®配合錠」についても、エンパグリフロジンの「2型糖尿病」に係る再審査期間と同一の2022年12月25日に再審査期間が終了している。
このように、リナグリプチン含有製剤である「トラゼンタ®錠」及び「トラディアンス®配合錠」は、いずれも薬事上の独占期間が既に終了している。しかしながら、現時点ではこれらを対象とする後発医薬品の製造販売承認は確認されていない。すなわち、薬事上の独占期間の終了後も、特許権が後発医薬品参入の実質的な障壁として機能している状況にあると考えられる。
リナグリプチン含有製剤に関連しては、存続期間延長登録出願がなされた特許を中心に一定数の特許群が形成されている。これらを整理すると、概ね一定の構造的傾向が認められる。詳細は以下の表(2026年1月12日時点のJ-PlatPat情報)に示すとおりである(なお、延長登録出願が行われていない関連特許が別途存在する可能性はある)。
例えば、本件特許第6143809号(表中7-4)は、「トラディアンス®配合錠」の承認に基づき特許権の存続期間が1年4月1日延長されている。他方、「トラゼンタ®錠」の承認に基づく延長はされておらず、満了日は2027年5月3日とされている。
| ファミリー | 特許番号 | 発明の名称 | 発明の概要 | 20年満了日 (無効審判有無) | +存続期間延長 |
|---|---|---|---|---|---|
| 1-1 | 4395304 | キサンチン誘導体、それらの調製及び医薬組成物としてのそれらの使用 | リナグリプチン物質 | 2022/02/21 | トラゼンタ錠承認で+1Y8M7D トラディアンス配合錠承認で+5Y |
| 1-2 | 5189883 | キサンチン誘導体、それらの調製及び医薬組成物としてのそれらの使用 | リナグリプチンとの併用配合医薬組成物 | 2022/02/21 | トラディアンス配合錠承認で+5Y |
| 2-1 | 4233524 | 8-[3-アミノ-ピペリジン-1-イル]-キサンチン、その製造およびその薬理組成物としての使用 | リナグリプチン物質 | 2023/08/18 | トラゼンタ錠承認で+2Y6M11D トラディアンス配合錠承認で+5Y |
| 2-2 | 4971251 | 8-[3-アミノ-ピペリジン-1-イル]-キサンチン、その製造およびその薬理組成物としての使用 | リナグリプチン併用医薬組成物 | 2023/08/18 | トラディアンス配合錠承認で+5Y |
| 2-3 | 5351486 | 8-[3-アミノ-ピペリジン-1-イル]-キサンチン、その製造およびその薬理組成物としての使用 | リナグリプチン物質 | 2023/08/18 | トラディアンス配合錠承認で+5Y |
| 3 | 4181605 | グルコピラノシル置換フェニル誘導体、該化合物を含有する医薬品及びその使用と製造方法 | エンパグリフロジン物質 | 2025/03/11 | トラディアンス配合錠承認で+5Y |
| 4 | 4226070 | 1-クロロ-4-(β-D-グルコピラノース-1-イル)-2-[4-((S)-テトラヒドロフラン-3-イルオキシ)-ベンジル]-ベンゼンの結晶性形態、その調製方法及び薬物を調製するためのその使用 | エンパグリフロジン結晶形 | 2026/05/02 | トラディアンス配合錠承認で+5Y |
| 5-1 | 5478244 | DPPⅣインヒビター製剤 | リナグリプチン製剤 | 2027/04/30 | トラディアンス配合錠承認で+4Y6M30D |
| 5-2 | 6100998 | DPPⅣインヒビター製剤 | リナグリプチン製剤 | 2027/04/30 | – |
| 5-3 | 6564720 | DPPⅣインヒビター製剤 | リナグリプチン製剤 | 2027/04/30 | – |
| 5-4 | 6987908 | DPPⅣインヒビター製剤 | リナグリプチン製剤 | 2027/04/30 | – |
| 5-5 | 7084711 | DPPⅣインヒビター製剤 | リナグリプチン製剤 | 2027/04/30 | – |
| 6-1 | 5323684 | 多形体 | リナグリプチン結晶形 | 2027/04/30 (訂正後維持審決) | トラディアンス配合錠承認で+5Y |
| 6-2 | 5800773 | 多形体 | リナグリプチン結晶形調整方法 | 2027/04/30 | – |
| 6-2 | 6022513 | 多形体 | リナグリプチン結晶形含有薬剤 | 2027/04/30 | トラディアンス配合錠承認で+1Y11M6D |
| 6-3 | 6309589 | 多形体 | リナグリプチン結晶形調整方法 | 2027/04/30 | – |
| 6-4 | 6602909 | 多形体 | リナグリプチン結晶形調整方法 | 2027/04/30 | – |
| 7-1 | 5734564 | DPPⅣインヒビターの使用 | リナグリプチン併用用量 | 2027/05/03 (無効審決) | トラディアンス配合錠承認で+3Y4M27D |
| 7-2 | 5813293 | DPPⅣインヒビターの使用 | リナグリプチン単離又は貯蔵用組成物 | 2027/05/03 (訂正後維持審決) | トラディアンス配合錠承認で+2Y11M18D |
| 7-3 | 5927146 | DPPⅣインヒビターの使用 | リナグリプチン特定用量と他剤との組合せ薬物 | 2027/05/03 (無効審決) | トラディアンス配合錠承認で+2Y4M23D |
| 7-4 | 6143809 | DPPⅣインヒビターの使用 | リナグリプチン特定用量/用途 | 2027/05/03 (無効審決/出訴) | トラディアンス配合錠承認で+1Y4M1D |
| 7-5 | 6662970 | DPPⅣインヒビターの使用 | リナグリプチン特定用量/特定患者用途 | 2027/05/03 (無効審判係属) | – |
| 7-6 | 6995822 | DPPⅣインヒビターの使用 | リナグリプチン特定用量/特定患者用途 | 2027/05/03 (維持審決) (非侵害判定) | – |
| 8 | 5595914 | グルコピラノシル置換ベンゼン誘導体を含有する医薬組成物 | リナグリプチンとエンパグリフロジンの糖尿病医薬組成物 | 2028/08/15 | トラディアンス配合錠承認で+4Y1M5D |
| 9-1 | 6290627 | メトホルミン治療に不適切な患者における糖尿病の治療 | リナグリプチン特定用量/特定患者用途 | 2029/08/05 (訂正後無効審決) | トラディアンス配合錠承認で+7M4D |
| 9-2 | 6480887 | メトホルミン治療に不適切な患者における糖尿病の治療 | リナグリプチン特定用量/特定患者用途 | 2029/08/05 (維持審決) | – |
| 10-1 | 6262023 | 経口又は非経口抗糖尿病薬による治療にもかかわらず不十分な血糖調節の患者の糖尿病の治療 | リナグリプチン特定用量/特定患者用途 | 2029/10/15 (維持審決/出訴) | – |
| 10-2 | 6811203 | 経口又は非経口抗糖尿病薬による治療にもかかわらず不十分な血糖調節の患者の糖尿病の治療 | リナグリプチン特定用量/特定患者用途 | 2029/10/15 (訂正後維持審決/出訴?) | – |
| 10-3 | 7174020 | 経口又は非経口抗糖尿病薬による治療にもかかわらず不十分な血糖調節の患者の糖尿病の治療 | リナグリプチン特定用量/特定患者用途 | 2029/10/15 (審判係属) | – |
| 11 | 5896276 | 1型糖尿病、2型糖尿病、耐糖能障害又は高血糖の治療用SGLT-2阻害薬 | エンパグリフロジン用量 | 2030/02/11 | トラディアンス配合錠承認で+2Y6M9D |
| 12 | 5456795 | リナグリプチン及び必要に応じてSGLT2阻害薬を含む医薬組成物、並びにその使用 | リナグリプチンとエンパグリフロジンの用量/個体医薬剤形 | 2030/02/11 | トラディアンス配合錠承認で+4Y8M3D |
| 13 | 6189374 | 糖尿病療法 | リナグリプチン用途医薬組成物とインスリン併用 | 2031/06/22 (維持審決/出訴) | トラディアンス配合錠承認で+1Y1M10D |
| 14-1 | 6177992 | エンパグリフロジンの治療的使用 | エンパグリフロジン特定患者用途 | 2034/04/03 | トラディアンス配合錠承認で+1Y1M30D |
| 14-2 | 6431959 | エンパグリフロジンの治療的使用 | エンパグリフロジン特定患者用途 | 2034/04/03 | – |
後発メーカーの動向を見ると、配合剤である「トラディアンス®配合錠」に関しては無効審判請求が行われていない。一方、リナグリプチン単剤である「トラゼンタ®錠5mg」を保護する残存特許(表中で発明の概要欄を赤字で示したもの)については、特に医薬用途発明に係る特許群に対して集中的に無効審判請求が行われている点が特徴的である。
これに対し、リナグリプチンの結晶形特許や製剤特許については無効審判請求がなされていない。したがって、後発メーカーは製剤設計等により、これら特許の技術的範囲を回避する方策を検討している可能性が高い。そして、医薬用途発明に係る特許群を無効とすることができれば、「トラゼンタ®錠5mg」の承認に基づいて存続期間が延長されたリナグリプチン物質特許が満了する2026年3月以降、後発医薬品としての承認取得が可能になるという戦略が想定される。
これら無効審判の審理は既に相当程度進んでおり、多くの事案では無効審決が確定している。現在残されている主要な争点は、特許第6143809号(沢井製薬を請求人、日本ジェネリックを参加人とする事案)や特許第6262023号(ニプロを請求人とする事案)など、特定患者群に特徴を有する用途特許の取扱いである。また、「トラゼンタ®錠5mg」の承認直前に出願された特許第6189374号については、審決取消訴訟の帰趨が注目される状況にある。
リナグリプチンは、単剤製品としての上市に始まり、SGLT2阻害薬エンパグリフロジンとの配合剤への展開、さらに再審査期間終了後を見据えた特許網の構築に至るまで、製品ライフサイクル全体を貫く戦略が極めて明瞭に表れた医薬品である。医薬品開発、薬事制度、特許制度がどのように相互に連関し、物質特許のみならず、結晶形発明、製剤発明、さらには適応症、用法用量、患者群に特徴を有する医薬用途発明といった特許群が、後発医薬品の参入時期や参入範囲にいかなる影響を及ぼし得るのか。本件は、その相互作用を検討する上で極めて示唆に富む事例といえる。
※ご覧いただきありがとうございます。この記事の内容について、読者の皆さまのご意見や気づきもぜひお聞かせください!
以下のようなご感想・質問、大歓迎です!
- 🤔ここ理解しづらいな、という部分はありましたか?
- 🤔このニュース、事件、判決例の実務影響についてご意見ありますか?
- 🤔過去の類似事例や判決例をご存じでしたら教えてください!
- 🤔恥ずかしい質問、つぶやき、大歓迎です
- 「👍」「なるほど」「疑問あり」だけでもOK!
コメント欄は↓ コメントは匿名OK! ぜひ気軽に投稿してください🙇
皆さんの反応が、次回の記事や解説のヒントになります🥰
Robot icons created by Freepik – Flaticon; Robot cat icons created by Freepik – Flaticon





コメント