2021年2月26日、武田薬品工業は、糖尿病治療薬4剤について、帝人ファーマに販売を移管するとともに、日本における製造販売承認及びこれに関連する資産を譲渡することを決定し、帝人及び帝人ファーマとの間で資産譲渡契約を締結したと発表しました。本記事は、本譲渡対象製品及び競合するDPP-4阻害剤製品を保護するそれぞれの基本特許(物質特許)に係る特許権存続期間満了時期の前後関係から、本譲渡対象製品の将来の売上推移は、そのジェネリックが市場に参入してくるよりもずっと前、むしろ競合品のジェネリックの市場参入により大きな影響を受ける可能性があることを確認したものです。帝人はここ数年内にさらに次の具体的なヘルスケア事業の成長施策や成果を打ち出していく必要があるでしょう。
- 1.プレスリリースの概要
- 2.本資産譲渡契約に至った両社の理由
- 3.本譲渡対象製品の物質特許
- 4.DPP-4阻害剤の競合品、ジェネリック登場は2025年前後以降か
- (1)エクア®錠(ビルダグリプチン)・エクメット®配合錠(ビルダグリプチン/メトホルミン塩酸塩)
- (2)ジャヌビア®錠(シタグリプチンリン酸塩水和物)・スージャヌ®配合錠(シタグリプチンリン酸塩水和物/イプラグリフロジンL−プロリン)・グラクティブ®錠(シタグリプチンリン酸塩水和物)
- (3)テネリア®錠(テネリグリプチン臭化水素酸塩水和物)・カナリア®配合錠(テネリグリプチン臭化水素酸塩水和物/カナグリフロジン水和物)
- (4)スイニー®錠(アナグリプチン)・メトアナ®配合錠(アナグリプチン/メトホルミン塩酸塩)
- (5)トラゼンタ®錠(リナグリプチン)・トラディアンス®配合錠(リナグリプチン/エンパグリフロジン)
- (6)オングリザ®錠(サキサグリプチン水和物)
- (7)マリゼブ®錠(オマリグリプチン)
- 5.まとめ
1.プレスリリースの概要
2021年2月26日、武田薬品工業は、DPP-4(ジペプチジルペプチダーゼ-4)阻害剤であるアログリプチン安息香酸塩(Alogliptin benzoate)またはトレラグリプチンコハク酸塩(Trelagliptin Succinate)を有効成分として含む以下の糖尿病治療薬4剤
- ネシーナ®錠6.25mg、同錠12.5mg、同錠25mg(一般名: アログリプチン安息香酸塩)
- リオベル®配合錠HD、同配合錠LD(一般名: アログリプチン安息香酸塩/ピオグリタゾン塩酸塩)
- イニシンク®配合錠(一般名: アログリプチン安息香酸塩/メトホルミン塩酸塩)
- ザファテック®錠25mg、同錠50mg、同錠100mg(一般名: トレラグリプチンコハク酸塩)
について、帝人ファーマに販売を移管するとともに、日本における製造販売承認及びこれに関連する資産を譲渡することを決定し、帝人及び帝人ファーマとの間で資産譲渡契約を締結したと発表しました。本譲渡対象製品の2020年3月期における日本国内における売上高は308億円であり、本資産譲渡価額は1,330億円となる見込み。
2021年4月1日付で販売移管を実行し、以後、武田薬品工業が引き続き当該製品を製造、帝人ファーマに供給、流通を担い、帝人ファーマが販売及び情報提供・収集活動を担うとのことです。本譲渡対象製品の製造販売承認権は当面の間武田薬品工業が引き続き保有し、承継時期については今後検討し決定していく予定。
- 2021.02.26 武田薬品工業 press release: 日本における糖尿病治療薬4剤の帝人ファーマ株式会社への販売移管及び製造販売承認の承継について
- 2021.02.26 帝人 press release: 2型糖尿病治療剤「ネシーナ®錠」、「リオベル®配合錠」、「イニシンク®配合錠」、「ザファテック®錠」の日本における販売移管、知的財産権実施許諾及び製造販売承認の承継に係る資産譲渡契約の締結に関するお知らせ
2.本資産譲渡契約に至った両社の理由
本資産譲渡の理由として、武田薬品工業は、プレスリリースの中で以下のように述べています。
現在、主要な5つのビジネスエリア(消化器系疾患、希少疾患、血漿分画製剤、オンコロジー、ニューロサイエンス)において最先端のイノベーションを追求しており、・・・今回の譲渡対象製品は、今後も患者さんのニーズを満たす重要な役割を担うものの、当社の長期的成長を牽引する主要ビジネスエリアの製品には該当しません。
武田薬品工業は、2016年に糖尿病領域の創薬研究からの撤退を発表しています。
一方、帝人は、プレスリリースの中で以下のように述べています。
「代謝・循環器領域」を注力疾患領域の1つとしている帝人ファーマにおいて、ブランド力のある本件対象製品の承継は、将来の事業拡大のための事業基盤の維持・強化を可能とするものです。また、こうした2型糖尿病治療剤を主要製品としてラインナップに加え、事業基盤を維持・強化することで、疾病治療への取り組みのみならず、当社グループが「Strategic Focus」として手掛ける生活習慣病の予防や重症化予防に貢献するサービスの拡大を加速できると考えています。
上記のような考えのもと、本件対象製品の獲得による製品ポートフォリオ拡充を通した事業基盤の強化、シナジー創出により、当社グループのヘルスケア事業の一層の成長を目指すことを目的として、本件対象製品の国内における製造販売承認を承継することといたしました。
現時点での帝人グループ・ヘルスケア事業にとっての最大の経営課題は、主力薬である高尿酸血症・痛風治療剤フェブリク®(一般名: フェブキソスタット)の後発品参入の影響を最小化すること、すなわち、フェブリク・パテントクリフによる売上収益の落ち込みを、新事業の拡大、医薬・在宅医療事業の生産性向上とコスト構造改革でカバーすることです(過去記事: 帝人・ヘルスケア(医薬品)事業の知的財産活動の景色(2020))。
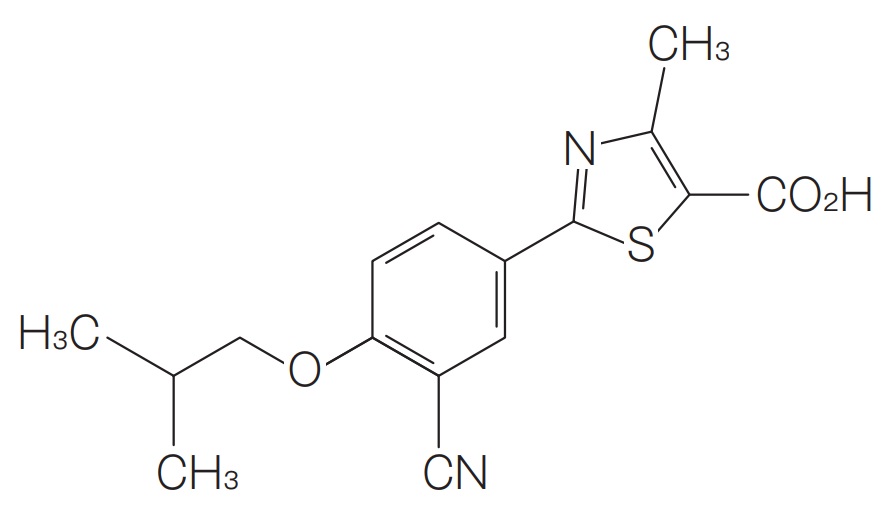
フェブリク®の再審査期間が2021年1月20日に終了したことで、フェブリク®のジェネリックが2022年2月に承認、6月の薬価収載・販売開始が想定されます。
さらに、フェブリク®の一部効能・効果を保護すると思われる用途特許に対して、日本ケミファ、日医工、沢井製薬がの無効審判を請求し(無効2020-800044、無効2020-800008)、虫食いではなくフル効能・効果でのジェネリック承認を狙っています。現在、無効2020-800044事件において、進歩性欠如を理由として特許を無効とする旨の審決の予告が出ています(2020年12月22日)。特許権者である帝人は窮地に立たされています。
帝人・ヘルスケア事業は、2022年以降に想定される主力品フェブリク®のパンテントクリフによる売上の落ち込みを、今回の承継製品群で何とか凌ぎ、事業基盤の維持と成長につなげたいところです。
3.本譲渡対象製品の物質特許
以下に、本譲渡対象製品を保護する物質特許に係る特許権存続期間満了時期を記しました。少なくとも下記時期までそれら製品のジェネリック市場参入の脅威は無いと見込まれます。
(1)ネシーナ®錠(アログリプチン安息香酸塩)
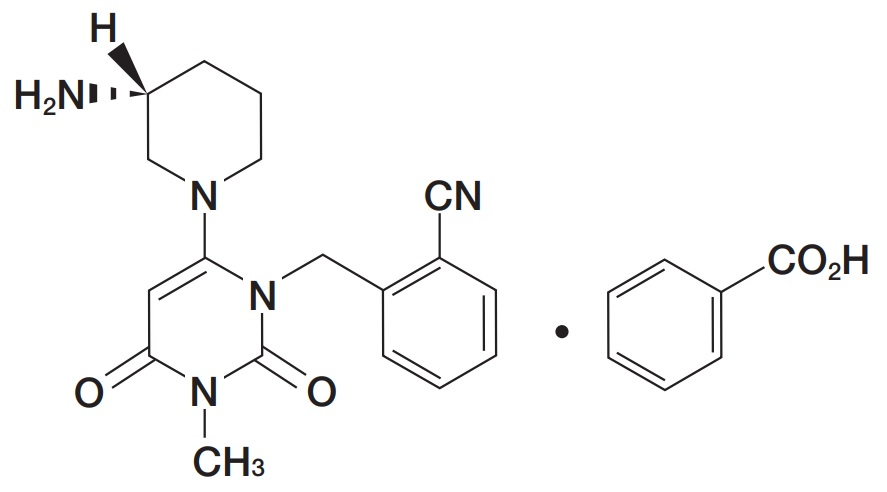 アログリプチンの物質特許3895349は、2024年12月17日で20年の満了となりますが、ネシーナ®錠の効能・効果(2型糖尿病の効果不十分療法への適応)各承認に基づいて複数の存続期間延長登録がなされたことにより、 2028年4月~2029年12月まで存続します。この物質特許及び延長登録が有効である限り、この時期までネシーナ®錠のジェネリックの市場参入はないと推測されます。
アログリプチンの物質特許3895349は、2024年12月17日で20年の満了となりますが、ネシーナ®錠の効能・効果(2型糖尿病の効果不十分療法への適応)各承認に基づいて複数の存続期間延長登録がなされたことにより、 2028年4月~2029年12月まで存続します。この物質特許及び延長登録が有効である限り、この時期までネシーナ®錠のジェネリックの市場参入はないと推測されます。
(2)イニシンク®配合錠(アログリプチン安息香酸塩/メトホルミン塩酸塩)
同アログリプチン物質特許は、イニシンク®配合錠の承認に基づいて5年の存続期間延長が認められ、2029年12月まで存続します。
(3)リオベル®配合錠(アログリプチン安息香酸塩/ピオグリタゾン塩酸塩)
同アログリプチン物質特許について、リオベル®配合錠の承認に基づいて延長登録の出願がなされましたが、先行処分の存在を理由に拒絶査定を受けました。拒絶査定不服審判が請求されましたが取下げられました。従って、リオベル®配合錠について、同特許による保護期間は2024年12月までとなります。
(4)ザファテック®錠(トレラグリプチンコハク酸塩)
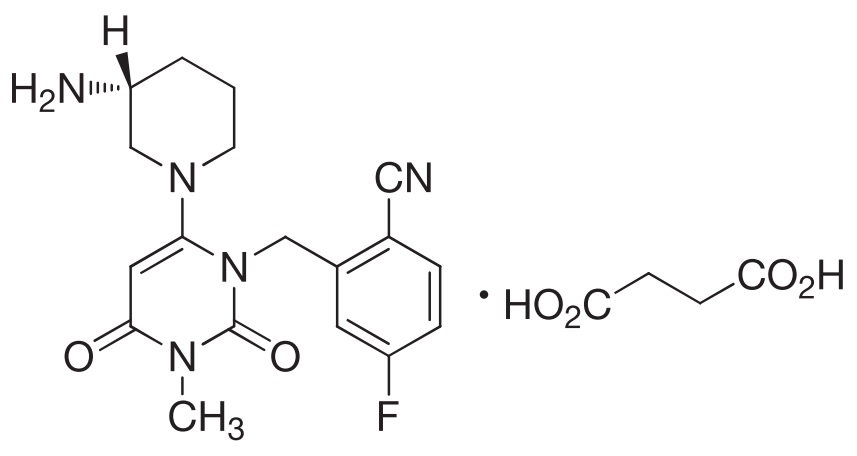 ザファテック®錠の有効成分であるトレラグリプチンの物質特許4068118は、アログリプチンの物質特許3895349の分割出願に由来しています。トレラグリプチン物質特許は、2024年12月で20年の満了となりますが、ザファテック®錠の承認に基づいて5年の存続期間延長が認められ、2029年12月まで存続します。
ザファテック®錠の有効成分であるトレラグリプチンの物質特許4068118は、アログリプチンの物質特許3895349の分割出願に由来しています。トレラグリプチン物質特許は、2024年12月で20年の満了となりますが、ザファテック®錠の承認に基づいて5年の存続期間延長が認められ、2029年12月まで存続します。
ザファテック®錠は、週1回投与の持続性選択的DPP-4阻害薬です。
4.DPP-4阻害剤の競合品、ジェネリック登場は2025年前後以降か
DPP-4阻害剤として本譲渡対象製品の競合品に当たる7社の製品群について、それぞれのDPP-4阻害剤である有効成分を保護する物質特許が満了する時期を以下に記しました。
その時期以降にこれらのジェネリックの市場参入の可能性があるわけですが、それらのタイミングが早ければ、競争環境はさらに厳しいものとなり、本譲渡対象製品群の売上推移は大きな影響を受けるかもしれません。
(1)エクア®錠(ビルダグリプチン)・エクメット®配合錠(ビルダグリプチン/メトホルミン塩酸塩)
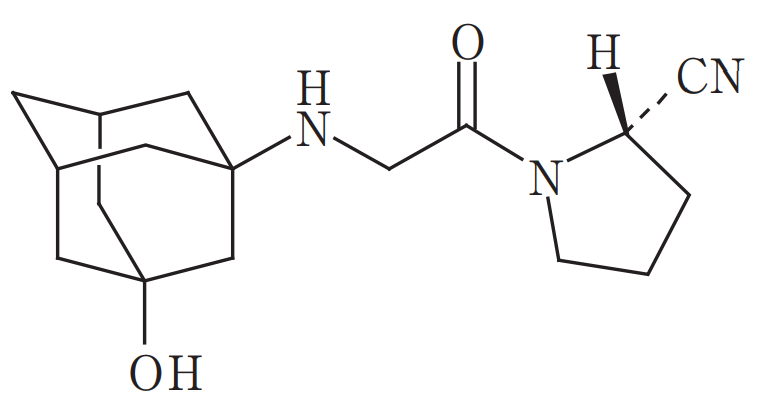 DPP-4阻害剤として本譲渡対象製品の競合品にあたる、エクア®錠(一般名: ビルダグリプチン(Vildagliptin))及びエクメット®配合錠(一般名: ビルダグリプチン/メトホルミン塩酸塩)(製造販売元: ノバルティスファーマ、販売元: 大日本住友製薬)を保護するビルダグリプチン物質特許3681110は、5年延長された存続期間が2024年12月9日に満了します。
DPP-4阻害剤として本譲渡対象製品の競合品にあたる、エクア®錠(一般名: ビルダグリプチン(Vildagliptin))及びエクメット®配合錠(一般名: ビルダグリプチン/メトホルミン塩酸塩)(製造販売元: ノバルティスファーマ、販売元: 大日本住友製薬)を保護するビルダグリプチン物質特許3681110は、5年延長された存続期間が2024年12月9日に満了します。
ビルダグリプチン物質特許以外に少なくとも製法や製剤に関する特許も存在しますが、ジェネリックメーカーがこれら技術を回避することに成功すれば、ビルダグリプチン物質特許が満了する2024年12月以降、すなわち、早ければ2025年中にはエクア®錠やエクメット®配合錠のジェネリックが市場参入する可能性があります。
エクア®錠及びエクメット®配合錠は、2019年にノバルティスファーマから大日本住友製薬に販売移管された経緯があります(2019.05.30 大日本住友製薬 press release: 糖尿病治療薬「エクア」および「エクメット」の日本における共同プロモーションおよび販売提携契約締結のお知らせ)。
(2)ジャヌビア®錠(シタグリプチンリン酸塩水和物)・スージャヌ®配合錠(シタグリプチンリン酸塩水和物/イプラグリフロジンL−プロリン)・グラクティブ®錠(シタグリプチンリン酸塩水和物)
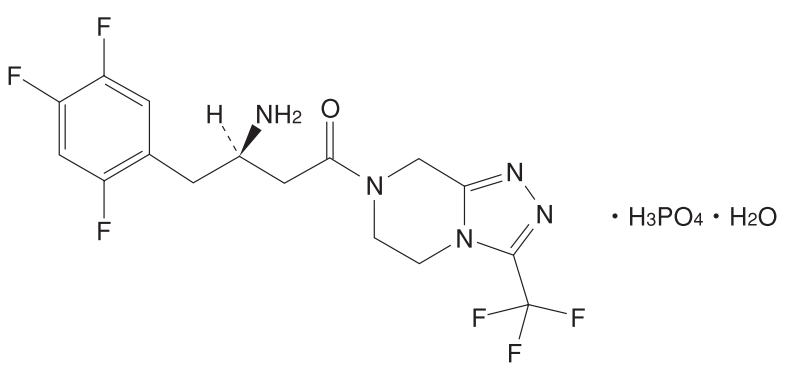 DPP-4阻害剤として本譲渡対象製品の競合品にあたる、ジャヌビア®錠(一般名: シタグリプチンリン酸塩水和物(Sitagliptin phosphate hydrate))及びスージャヌ®配合錠(一般名: シタグリプチンリン酸塩水和物/イプラグリフロジンL−プロリン)(製造販売元: MSD)を保護するシタグリプチン物質特許3762407(20年の満了日: 2022年7月5日)は、ジャヌビア®錠について延長された存続期間が2025年2月21日~2026年3月30日(効能・効果による)に、スージャヌ®配合錠について延長された存続期間が2027年7月5日に満了します。
DPP-4阻害剤として本譲渡対象製品の競合品にあたる、ジャヌビア®錠(一般名: シタグリプチンリン酸塩水和物(Sitagliptin phosphate hydrate))及びスージャヌ®配合錠(一般名: シタグリプチンリン酸塩水和物/イプラグリフロジンL−プロリン)(製造販売元: MSD)を保護するシタグリプチン物質特許3762407(20年の満了日: 2022年7月5日)は、ジャヌビア®錠について延長された存続期間が2025年2月21日~2026年3月30日(効能・効果による)に、スージャヌ®配合錠について延長された存続期間が2027年7月5日に満了します。
スージャヌ®配合剤については、もう一方の有効成分であるイプラグリフロジンL−プロリン(SGLT-2阻害剤)の物質特許4222450において5年延長登録が存在します(2029年3月12日満了)。
ジャヌビア®錠を保護するものとして、シタグリプチン物質特許以外に少なくとも結晶に関する特許も存在しますが、ジェネリックメーカーがこれら技術を回避するか特許を無効にすることに成功すれば、シタグリプチン物質特許が満了する2025年2月以降にはジャヌビア®錠のジェネリックが虫食いの効能・効果で市場参入する可能性があります。
グラクティブ®錠(製造販売元: 小野薬品工業)は、ジャヌビア®錠と同じシタグリプチンリン酸塩水和物を有効成分とするものであることから、シタグリプチン物質特許3762407で保護される製品ですが、同特許の存続期間延長登録出願はされていません。
(3)テネリア®錠(テネリグリプチン臭化水素酸塩水和物)・カナリア®配合錠(テネリグリプチン臭化水素酸塩水和物/カナグリフロジン水和物)
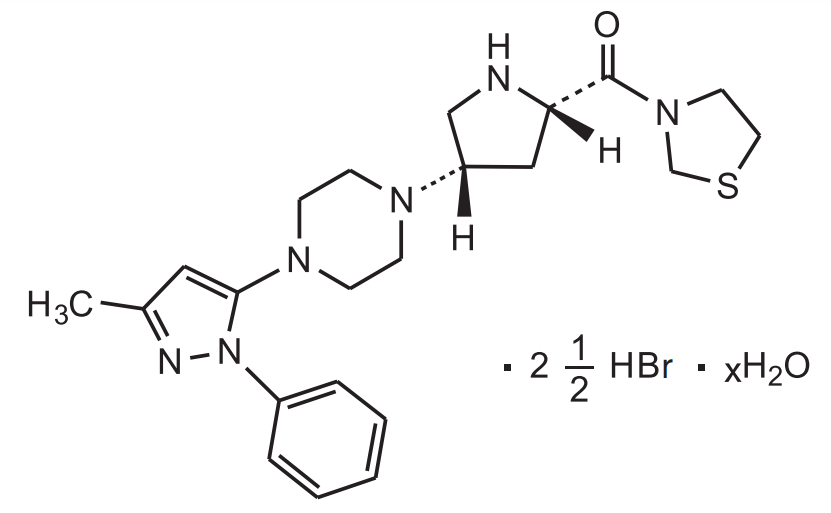 DPP-4阻害剤として本譲渡対象製品の競合品にあたる、テネリア®錠(一般名: テネリグリプチン臭化水素酸塩水和物(Teneligliptin Hydrobromide Hydrate))及びカナリア®配合錠(一般名: テネリグリプチン臭化水素酸塩水和物/カナグリフロジン水和物)(製造販売元: 田辺三菱製薬、販売元: 第一三共)を保護するテネリグリプチン物質特許4101053(20年の満了日: 2021年8月10日)は、テネリア®錠について延長された存続期間が2025年11月10日又は2026年8月10日(効能・効果による)に、カナリア®配合錠について延長された存続期間が2026年8月10日に満了します。
DPP-4阻害剤として本譲渡対象製品の競合品にあたる、テネリア®錠(一般名: テネリグリプチン臭化水素酸塩水和物(Teneligliptin Hydrobromide Hydrate))及びカナリア®配合錠(一般名: テネリグリプチン臭化水素酸塩水和物/カナグリフロジン水和物)(製造販売元: 田辺三菱製薬、販売元: 第一三共)を保護するテネリグリプチン物質特許4101053(20年の満了日: 2021年8月10日)は、テネリア®錠について延長された存続期間が2025年11月10日又は2026年8月10日(効能・効果による)に、カナリア®配合錠について延長された存続期間が2026年8月10日に満了します。
カナリア®配合剤については、もう一方の有効成分であるカナグリフロジン(SGLT-2阻害剤)の物質特許や製剤特許なども存在します。
テネリア®錠を保護するものとして、テネリグリプチン物質特許以外に少なくとも結晶に関する特許も存在しますが、ジェネリックメーカーがこれら技術を回避するか特許を無効にすることに成功すれば、テネリグリプチン物質特許が満了する2025年11月以降にはテネリア®錠のジェネリックが虫食い効能・効果で市場参入する可能性があります。
(4)スイニー®錠(アナグリプチン)・メトアナ®配合錠(アナグリプチン/メトホルミン塩酸塩)
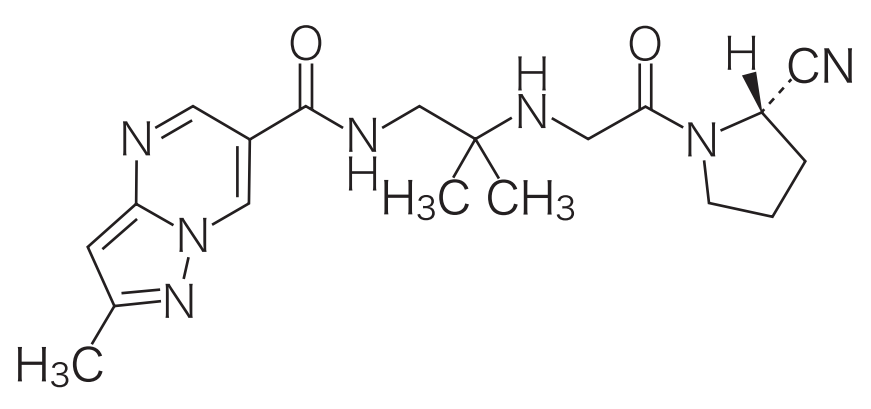 DPP-4阻害剤として本譲渡対象製品の競合品にあたる、スイニー®錠(一般名: アナグリプチン(Anagliptin))及びメトアナ®配合錠(一般名: アナグリプチン/メトホルミン塩酸塩)(製造販売元: 三和化学研究所、スイニー®錠販売元: 興和)を保護するアナグリプチン物質特許4184378(20年の満了日: 2024年1月30日)は、スイニー®錠について延長された存続期間が2027年1月24日又は2028年2月14日に(効能・効果による)、メトアナ®配合錠について延長された存続期間が2029年1月30日に満了します。
DPP-4阻害剤として本譲渡対象製品の競合品にあたる、スイニー®錠(一般名: アナグリプチン(Anagliptin))及びメトアナ®配合錠(一般名: アナグリプチン/メトホルミン塩酸塩)(製造販売元: 三和化学研究所、スイニー®錠販売元: 興和)を保護するアナグリプチン物質特許4184378(20年の満了日: 2024年1月30日)は、スイニー®錠について延長された存続期間が2027年1月24日又は2028年2月14日に(効能・効果による)、メトアナ®配合錠について延長された存続期間が2029年1月30日に満了します。
スイニー®錠を保護するものとして、アナグリプチン物質特許以外に少なくとも結晶に関する特許等も存在しますが、ジェネリックメーカーがこれら技術を回避するか特許を無効にすることに成功すれば、アナグリプチン物質特許が満了する2027年以降にはスイニー®錠のジェネリックが虫食い効能・効果で市場参入する可能性があります。
(5)トラゼンタ®錠(リナグリプチン)・トラディアンス®配合錠(リナグリプチン/エンパグリフロジン)
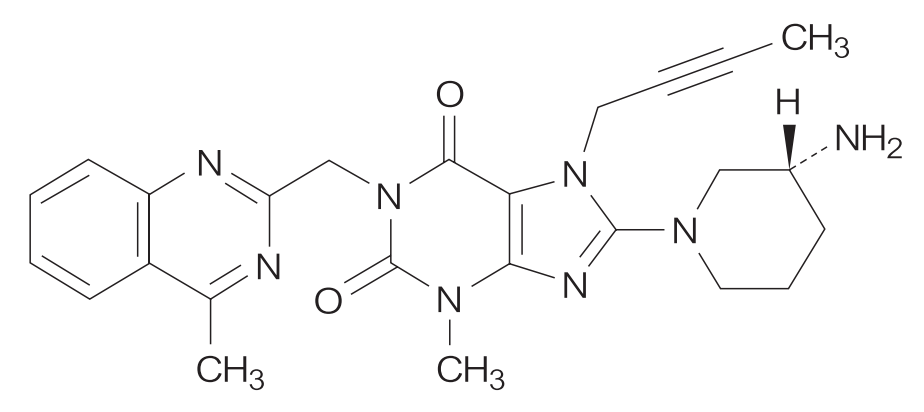 DPP-4阻害剤として本譲渡対象製品の競合品にあたる、トラゼンタ®錠(一般名: リナグリプチン(Linagliptin))及びトラディアンス®配合錠(一般名: リナグリプチン/エンパグリフロジン)(製造販売元: 日本ベーリンガーインゲルハイム)を保護するリナグリプチン物質特許 4395304(20年の満了日: 2022年2月21日)及び4233524(20年の満了日: 2023年8月18日)は、トラゼンタ®錠について延長された存続期間がそれぞれ2023年10月28日及び2026年3月1日、トラディアンス®配合錠について延長された存続期間が2027年2月21日及び2028年8月18日に満了します。
DPP-4阻害剤として本譲渡対象製品の競合品にあたる、トラゼンタ®錠(一般名: リナグリプチン(Linagliptin))及びトラディアンス®配合錠(一般名: リナグリプチン/エンパグリフロジン)(製造販売元: 日本ベーリンガーインゲルハイム)を保護するリナグリプチン物質特許 4395304(20年の満了日: 2022年2月21日)及び4233524(20年の満了日: 2023年8月18日)は、トラゼンタ®錠について延長された存続期間がそれぞれ2023年10月28日及び2026年3月1日、トラディアンス®配合錠について延長された存続期間が2027年2月21日及び2028年8月18日に満了します。
トラディアンス®配合剤については、もう一方の有効成分であるエンパグリフロジン(SGLT-2阻害剤)の物質特許や製剤特許なども存在します。
トラゼンタ®錠を保護するものとして、リナグリプチン物質特許以外に少なくとも結晶に関する特許等も存在しますが、ジェネリックメーカーがこれら技術を回避するか特許を無効にすることに成功すれば、リナグリプチン物質特許が満了する2026年以降にはトラゼンタ®錠のジェネリックが市場参入すると想定されます。
(6)オングリザ®錠(サキサグリプチン水和物)
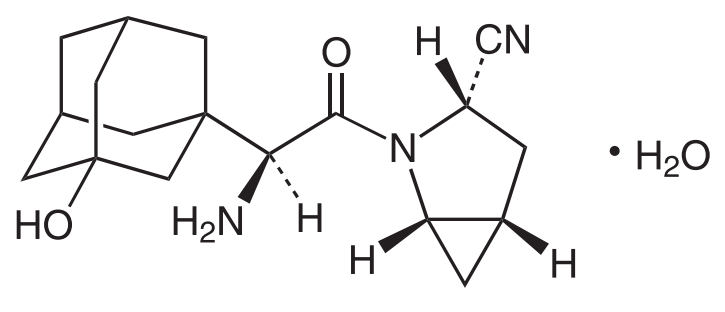 DPP-4阻害剤として本譲渡対象製品の競合品にあたる、オングリザ®錠(一般名: サキサグリプチン水和物(Saxagliptin Hydrate))(製造販売元: 協和キリン)を保護するサキサグリプチン物質特許4460205(20年の満了日: 2021年3月5日、アストラゼネカ社)は、延長された存続期間が2024年4月10日に満了します。もうひとつの物質特許4886193も延長登録を受けましたが年金不納による抹消となっています。
DPP-4阻害剤として本譲渡対象製品の競合品にあたる、オングリザ®錠(一般名: サキサグリプチン水和物(Saxagliptin Hydrate))(製造販売元: 協和キリン)を保護するサキサグリプチン物質特許4460205(20年の満了日: 2021年3月5日、アストラゼネカ社)は、延長された存続期間が2024年4月10日に満了します。もうひとつの物質特許4886193も延長登録を受けましたが年金不納による抹消となっています。
オングリザ®錠を保護するものとして、サキサグリプチン物質特許以外に少なくとも製剤に関する特許も存在(2026年8月6日に満了)しますが、ジェネリックメーカーがこれら技術を回避するか特許を無効にすることに成功すれば、サキサグリプチン物質特許が満了する2024年以降にはオングリザ®錠のジェネリックが市場参入すると想定されます。
(7)マリゼブ®錠(オマリグリプチン)
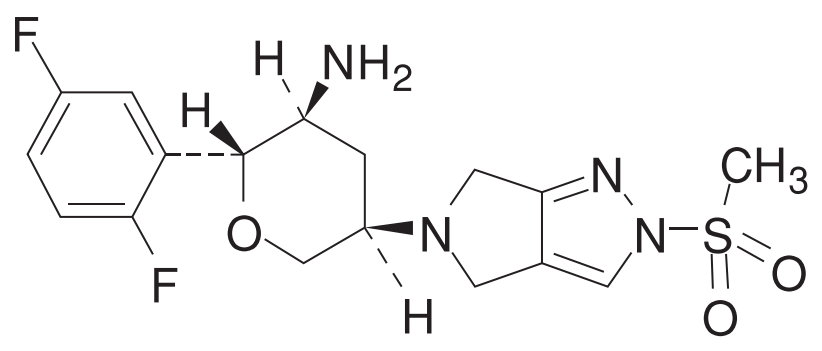 DPP-4阻害剤として本譲渡対象製品の競合品にあたる、マリゼブ®錠(一般名: オマリグリプチン(Omarigliptin))(製造販売元: MSD、販売元: キッセイ薬品)を保護するオマリグリプチン物質特許4854825(20年の満了日: 2029年11月11日、MSD社)は、延長された存続期間が2033年10月4日に満了します。マリゼブ®錠は、週1回投与の持続性選択的DPP-4阻害薬として2015年11月に世界に先駆けて日本で発売を開始しました。
DPP-4阻害剤として本譲渡対象製品の競合品にあたる、マリゼブ®錠(一般名: オマリグリプチン(Omarigliptin))(製造販売元: MSD、販売元: キッセイ薬品)を保護するオマリグリプチン物質特許4854825(20年の満了日: 2029年11月11日、MSD社)は、延長された存続期間が2033年10月4日に満了します。マリゼブ®錠は、週1回投与の持続性選択的DPP-4阻害薬として2015年11月に世界に先駆けて日本で発売を開始しました。
MSDは、2020年4月よりキッセイ薬品に販売移管することを決定した経緯があります(2020.02.03 キッセイ薬品 press release: 2型糖尿病治療薬「マリゼブ®」の販売移管に関するお知らせ)。
5.まとめ
長期的成長を牽引する主要ビジネスエリアへの選択と集中を推し進めたい武田薬品工業と、2022年に想定されるフェブリク®のパンテントクリフを凌いで次のヘルスケア事業基盤の維持と成長に繋げたい帝人との思惑が一致したことで、日本における糖尿病治療薬4剤(ネシーナ®錠、イニシンク®配合錠、リオベル®配合錠、ザファテック®錠)の販売移管及び資産譲渡契約の締結に至りました。
本譲渡対象製品を保護する基本特許(物質特許)の存在は、2028年4月~2029年12月までそれら製品のジェネリックが市場に参入することを一定程度阻止すると思われますが、むしろ同じDPP-4阻害剤である競合品の物質特許が早ければ2025年前後から次々と満了するため、それら競合品のジェネリックが早期に市場参入してくる可能性があります。
従って、本譲渡対象製品群の将来の売上推移は、それらの特許権の満了により製品寿命を全うするよりもずっと前、むしろ競合品のジェネリック市場参入により大きな影響を受けてしまうと想像されます。
国内の糖尿病治療薬市場は今後縮小に転じる見込みとの市場予測や、DPP-4阻害薬やSGLT-2阻害薬が特許切れを迎え、後発医薬品に置き換わっていくとの分析もあります。
「2024年までは市場は堅調に拡大するが、2025年以降は大型品の特許が切れ、ジェネリック医薬品が普及することから、市場縮小が予想される。」
– 2020.10.09 富士経済 press release「生活習慣病領域や腎疾患治療剤、その他循環器疾患治療剤の国内市場を調査」
「治療薬市場は、DPP-4阻害薬やSGLT2阻害薬が市場をけん引することで、拡大基調にある。ただ、先発品の特許切れに伴い、安価なジェネリック医薬品が一層普及することや、各社が開発を進める糖尿病の新薬候補の減少傾向などを鑑みると、市場は今後5年以内に縮小に転じると予測する。」
– 2020.08.07 矢野経済研究所「糖尿病市場に関する調査を実施(2020年)」
「DPP-4阻害薬やSGLT2阻害薬が特許切れを迎え、後発医薬品に置き換わっていく一方、各社のパイプラインを見てもこれらに続く大型の新薬候補はほとんどありません。」
– 2020.03.18 AnswersNews「糖尿病 迫る市場の縮小…相次ぐ事業見直しの一方、大日本住友は国内事業の柱に」
2020年3月期国内売上308億円である本譲渡対象製品に対して、本資産譲渡価額は1,330億円となる見込み。この販売移管及び資産譲渡契約が、帝人・ヘルスケア事業基盤の維持と成長につながる決断だったと評価されるためには、帝人はここ数年内にさらに次の具体的なヘルスケア事業の成長施策や成果を打ち出していく必要があるでしょう。


コメント
2021.03.20 日経メディカル「DPP-4阻害薬+メトホルミン」がTOP3を独占
1位はエクメット、2位はイニシンク、3位はメトアナ
https://medical.nikkeibp.co.jp/leaf/mem/pub/series/survey/202103/569569.html
2021.03.24 AnswersNews 「糖尿病治療薬 相次ぐ撤退で変わる勢力図…武田「ネシーナ」など売却」
https://answers.ten-navi.com/pharmanews/20723/
2023年8月15日に、シタグリプチンリン酸塩(後発品)が承認されています。
シタグリプチン物質特許3762407がジャヌビア錠の承認に基づいて延長されているがグラクティブ錠の承認に基づいては延長されていないということですが、今回の後発品の承認はグラクティブ錠をレファレンスとする後発品であって、ジャヌビア錠の承認に基づいて延長された特許権の効力が及ばないと厚労省が判断したということでしょうか?
もしそうだとすると、先発メーカーの大チョンボ及びその穴を突いた後発1社の優れた知財分析力ということになりますね。。。
コメントありがとうございます。グラクティブ錠の承認に基づいて特許延長されていない点については気になっていました。どのようなことが原因で今回の後発承認となったのかしばらく様子を見ましょう。