Summary
本件は、リパスジル製剤の光安定化に関する特許の特許権者である興和(原告)が、当該特許を進歩性欠如を理由として無効とした審決(請求人:東亜薬品)の取消しを求めた事案である。知財高裁は、原告主張の取消事由はいずれも理由がないとして請求を棄却した。
本判決は、医薬品分野における進歩性判断、とりわけ「効果」の位置付けに重要な示唆を与えるものである。
第一に、薬事承認のために必ず実施される試験によって当然に確認される性質、すなわち規制上の要請に基づき「おのずと明らかになる性質」にすぎない効果は、顕著な効果として進歩性を基礎付けるものとはならないことを明確にした。この点は、光安定性という本件固有の事情にとどまらず、医薬品開発において必須的に検証される各種品質特性等一般に広く影響し得る。
第二に、効果を明示しない物の発明と、「光安定性を向上させる方法」と明示した用途形式の発明とで結論が変わらなかった点も注目される。裁判所は、当該効果を独立の技術的意義を有する構成とは評価せず、既存構成に内在する通常の効果を表現したにとどまると整理した。すなわち、「効果の構成化」による形式的な差別化のみでは、進歩性を基礎付けることはできないとの立場を示したものと読める。
医薬系特許実務において、どの効果が「通常の効果」にとどまり、どの効果が技術的意義を有する新たな属性と評価され得るのか、その峻別がこれまで以上に重要になることを示唆する判決といえよう。
☕AIアシスタントたちのおしゃべりコーヒータイム☕
おや、ピポとミャオがおしゃべりしてますよ・・・

この部屋さ、遮光カーテンにしたら快眠できるよ。出願したら特許とれるかな?

遮光は容易想到ですね。

でも「すぐ寝れる」って顕著な効果じゃない?

それ、遮光すれば普通に内在してません?

「内在」?

試験すれば「おのずと明らか」になるタイプです。

じゃあさ、『この部屋でピポの睡眠の質を向上させる方法』ってクレームは?

用途形式にしても、中身は同じ、「新たな属性」を見出していませんよ。

「新たな属性」?

ピポ先輩、知らないんですか~? …っていうか、この部屋、オフィスですよ!

・・・
1.背景
本件(知財高裁令和7年(行ケ)10073)は、発明の名称を「医薬品」とする特許第6244038号の特許権者である興和株式会社(原告)が、当該特許を無効とした審決(請求人:東亜薬品株式会社(被告))の取消しを求めた事案である。争点は、進歩性判断の当否である。
(1)本件各訂正発明
本件訂正後の特許請求の範囲(本件各訂正発明)の請求項1及び9は以下のとおりである(その他請求項は省略)。
【請求項1】
リパスジル若しくはその塩又はそれらの溶媒和物を含有する水性組成物が、一次包装体に収容されてなり、
水性組成物中のリパスジル若しくはその塩又はそれらの溶媒和物の含有量が、水性組成物全容量に対して、フリー体換算で0.05~5w/v%であり、
前記一次包装体の内表面の総面積に対し50%以上の部分が、波長300~335nmの光線の透過率の平均値が10%以下となるように当該光線を遮断するものであり、
前記平均値は、波長300~335nmの範囲内において0.5nm毎に空気中での包装体の光透過率を分光光度計で測定した後にその平均値を算出することにより測定される値である、医薬製剤。
【請求項9】
リパスジル若しくはその塩又はそれらの溶媒和物を含有する水性組成物を、一次包装体に収容する工程を含み、
水性組成物中のリパスジル若しくはその塩又はそれらの溶媒和物の含有量が、水性組成物全容量に対して、フリー体換算で0.05~5w/v%であり、
前記一次包装体の内表面の総面積に対し50%以上の部分が、波長300~335nmの光線の透過率の平均値が10%以下となるように当該光線を遮断するものであり、
前記平均値は、波長300~335nmの範囲内において0.5nm毎に空気中での包装体の光透過率を分光光度計で測定した後にその平均値を算出することにより測定される値である、リパスジル若しくはその塩又はそれらの溶媒和物の水性組成物中での光安定性を向上させる方法。
眼科用剤等は、通常、水を含有する組成物(水性組成物)であるが、リパスジルを眼科用剤等として製剤化するに当たり、リパスジルの光安定性を評価したところ、リパスジル自体は光に対して安定であるにもかかわらず、これを水性組成物中に配合するによって光に対して不安定化し、曝光によって徐々に分解物が増加することが明らかとなったことから、リパスジルの水性組成物中での光に対する安定性を改善する技術を提供することが課題であった。本件各訂正発明は、リパスジルを含有する水性組成物を、300nm付近の波長の光線を遮断する包装体に収容することでこの課題を解決し、光安定性の改善された医薬製剤を提供できるという効果を奏するものであり、医薬品産業等において好適に利用できるという産業上の利用可能性を有するものである。
本件訂正発明1は、「医薬製剤」の発明であり、本件訂正発明9は、「リパスジルの水性組成物中での光安定性を向上させる方法」の発明である点で相違するが、その他の構成は概ね同一である。
(2)無効理由の主引用例甲2との関係
被告(東亜薬品)が請求した無効審判(無効2023-800005号)では、甲2(Current Eye Research, 2014年, Vol.39, No.8, pp.813-822)を主引用例とする進歩性欠如が主要な争点となった。
甲2は、ROCK阻害薬K-115(リパスジル塩酸塩水和物)の局所点眼液が新規かつ強力な抗緑内障薬であることを示した、原告(興和)研究者を著者とする論文であり、2014年2月6日にオンライン公開されている。本件特許の優先日は2014年9月25日であり甲2の公開後であった。
本件訂正発明1と甲2発明1(K-115を含有する局所点眼液)との一致点・相違点は以下のとおりである。
リパスジル若しくはその塩又はそれらの溶媒和物を含有する組成物。
(相違点1)
本件訂正発明1は、組成物が「水性組成物」であるのに対し、甲2発明1では、対応する事項が特定されていない点。
(相違点2)
本件訂正発明1は、組成物が「一次包装体に収容されてなり、前記一次包装体の内表面の総面積に対し50%以上の部分が、波長300~335nmの光線の透過率の平均値が10%以下となるように当該光線を遮断するものであり、前記平均値は、波長300~335nmの範囲内において0.5nm毎に空気中での包装体の光透過率を分光光度計で測定した後にその平均値を算出することにより測定される値である、医薬製剤」であるのに対し、甲2発明1では、対応する事項が特定されていない点。
本件訂正発明9と甲2発明2(K-115を、K-115点眼液のビヒクルに溶解させる工程からなる、K-115を含有する局所点眼液製造方法)との一致点・相違点は以下のとおりである。
リパスジル若しくはその塩又はそれらの溶媒和物を含有する組成物を容器に収容する工程を含む、方法。
(相違点4)
本件訂正発明9は、組成物が「水性組成物」であるのに対し、甲2発明2では、対応する事項が特定されていない点。
(相違点5)
「容器に収容する工程を含む、方法」について、本件訂正発明9では容器が「前記一次包装体の内表面の総面積に対し50%以上の部分が、波長300~335nmの光線の透過率の平均値が10%以下となるように当該光線を遮断するものであり、前記平均値は、波長300~335nmの範囲内において0.5nm毎に空気中での包装体の光透過率を分光光度計で測定した後にその平均値を算出することにより測定される値である」「一次包装体」であり、方法が「水性組成物中での光安定性を向上させる方法」であるのに対し、甲2発明2では、容器の材質が特定されない「局所点眼液製造方法」である点。
審決は、本件各訂正発明はいずれも甲2記載発明及び周知技術に基づいて当業者が容易に想到し得たものであり、特許法29条2項(進歩性欠如)に該当すると判断した。
これに対し原告は、本件審決の取消しを求めて本件訴訟を提起し、本件各訂正発明と甲2発明との相違点に係る容易想到性及び顕著な効果の判断に誤りがあると主張した。
2.裁判所の判断
2026年2月10日、知的財産高等裁判所第1部(以下「裁判所」)は、原告が主張する取消事由はいずれも理由がないとして、原告の請求は理由がないからこれを棄却することとし、主文のとおり判決した。
1 原告の請求を棄却する。
2 訴訟費用は原告の負担とする。
本判決は、主引用例である甲2(K-115/リパスジルに関する論文)に基づき、本件各訂正発明の相違点、すなわち①水性組成物である点(相違点1や相違点4)、②300~335nmの光線を遮断する包装体に収容する点(相違点2や相違点5)について、当業者が容易に想到し得たか、また主張された光安定性向上効果が顕著な効果といえるかを中心に判断したものである。
まず、本件各訂正発明の課題について、裁判所は、本件明細書の記載に基づき、リパスジル自体は光に安定であるにもかかわらず、水性組成物中に配合すると光によって分解物が増加することが判明したことから、水性組成物中での光安定性を改善することが課題であり、その解決手段として、300nm付近の波長の光線を遮断する包装体に収容する構成が採用されたものであると整理した。
(1)相違点1(水性組成物である点)
裁判所は、甲2においてK-115(リパスジル塩酸塩水和物)がTris-HCl緩衝液中で活性試験されていること、動物実験において局所点眼液が用いられていること等から、当業者は当該点眼液を水性組成物と理解すると認定した。
したがって、相違点1は実質的な相違点とはいえないか、仮に相違点であっても容易想到であると判断した。
(2)相違点2(300~335nmの光線を遮断する包装体への収容)
裁判所は、リパスジルを有効成分とする点眼薬について薬事承認を得るためには、光安定性を含む安定性試験を行い、必要に応じて容器の変更を繰り返すことが求められると認定した。そのため、当業者には、曝光の影響を受けない容器を選択しようとする動機付けがあるとした。
また、文献(甲12)には、薬物が不安定となる波長に応じて適切な遮光特性を有する点眼瓶等を選択する旨の記載があることから、遮光による安定性確保は周知の技術的手段であるとした。
原告は、波長300~335nmの光透過率平均値10%以下との数値限定には臨界的意義があると主張したが、裁判所は、提出図面(甲77図A)からは透過率の低減に応じて類縁物質が概ね比例的に減少する傾向が読み取れるにすぎず、10%前後で顕著な差があるとは認められないとした。したがって、当該数値限定は、当業者が安定性試験の結果に応じて適宜設定し得る範囲にとどまり、臨界的意義を有するものとはいえないと判断した。
さらに、優先日当時、ポリエチレン又はポリプロピレン製容器、紫外線吸収剤を配合した容器、遮光袋等の遮光手段は周知であり、当業者が容易に入手可能であったと認定した。
以上を踏まえ、裁判所は、当業者は許容される類縁物質量に応じて光透過率を適宜設定し、それに適した容器や包装を設計することにより、本件訂正発明1の構成に容易に到達し得たと結論付けた。
(3)顕著な効果
本件明細書には、紫外線吸収剤を含有するポリプロピレン製容器や、酸化チタン含有シュリンクフィルムを用いた容器では、透明容器に比べて類縁物質の生成が抑制される旨の試験結果が記載されている。
しかし裁判所は、薬物が特定波長の光により不安定となり得ることは周知であり、薬事承認に際して行われる光安定性試験(D65ランプ等、積算照射量120万lux・hr等)も周知の条件であると認定した。
そのため、300nm以上の光を一定程度遮断する容器に収容すれば透明容器より劣化が抑制されるという効果は、当業者が予測し得る程度の効果であり、「当業者が必ず行う製剤の光安定性試験によっておのずと明らかになる性質を確認したにすぎないものである」と指摘した。数値範囲の特定についても、前記のとおり臨界的意義は認められないとした。
(4)小括
以上のとおり、裁判所は、本件訂正発明1は甲2発明1及び周知技術に基づき当業者が容易に想到し得たものであると判断した(本件訂正発明2~7についても同様)。
(5)本件訂正発明9
本件訂正発明9は、「リパスジルをフリー体換算で0.05~5w/v%含有する水性組成物中のリパスジルの光安定性を向上させる方法」に関する発明であり、特定の一次包装体(内表面総面積の50%以上が、波長300~335nmの光透過率平均10%以下となるよう遮断するもの)に収容する工程を含む方法発明である。
裁判所は、まず、相違点4及び相違点5のうち容器に関する部分、並びに顕著な効果の評価については、前記訂正発明1と同様であるとした。その上で、原告は本件訂正発明9は特定の一次包装体の「新たな属性」を見出したことに基づく用途発明であると主張したが、裁判所はこれを採用しなかった。
すなわち、リパスジルを含有する水性組成物を一次包装体に収容することにより光安定性が向上することは、遮光容器を用いることによる「通常の効果」にすぎず、当該一次包装体の「新たな属性」を見出したものとはいえないと判断した。したがって、本件訂正発明9も、甲2発明2及び周知技術に基づき当業者が容易に想到し得たものであるとした(本件訂正発明10についても同様)。
(6)結論
以上のとおり、裁判所は、訂正発明1~10のいずれについても、甲2及び周知技術に基づき当業者が容易に想到し得たものであり、顕著な効果も認められないと判断した。そして、原告の主張する取消事由はいずれも理由がないとして、審決取消請求を棄却した。
3.コメント
(1)必ず行う試験によっておのずと明らかになる性質
本判決が示した重要なポイントの一つは、「薬事承認のために必ず実施される光安定性試験によっておのずと明らかになる性質を確認したにすぎない効果」は、顕著な効果として評価することはできないと明確に述べた点にある。
この射程は、本件のような遮光技術に限定されるものではない。医薬品の承認取得の過程において、規制上当然に確認され、かつ満たすことが前提とされている性質については、それが結果として明らかになったとしても、当業者にとって予測・期待の範囲内にある「通常の効果」にとどまると評価され得ることを示唆するものといえる。
すなわち、本判決は、規制実務において不可避的に実施される試験と技術常識との関係を、進歩性判断の枠組みに明示的に組み込んだ点に意義がある。
医薬品開発において各種品質特性等の評価は承認上不可欠であるが、これらの評価過程で把握される性質が直ちに創作的価値を基礎付けるわけではないことを、本判決は改めて確認したといえる。
(2)効果的記載と進歩性
本判決でもう一つ注目すべきは、構成として効果を明示しない本件訂正発明1と、「光安定性を向上させる方法」と明示した本件訂正発明9の双方について、結論が同一となった点である。
理論上は、効果的記載を構成要件として位置付けることにより、引用発明との差異を構成面で把握し、容易想到性判断を再構成する余地はあり得る。実際、効果に係る発明特定事項を相違点として評価し、進歩性を肯定した裁判例も存在する。
例えば、引用文献に特許発明の作用又は効果が内在していたとしても、それが明示又は意図されていない限り進歩性否定の根拠とはならないとした事例として、「高純度PTH含有凍結乾燥製剤及びその製造方法」事件がある(2024.12.07ブログ記事「2024.09.26 「旭化成ファーマ v. 沢井製薬」 大阪地裁令和4年(ワ)3344 ― 引用文献に明示されていない酸化抑制の構成を相違点と認定し、内在理論に基づいた容易想到性を否定した事例 ―」(『医薬系特許的判例ブログ年報 2024』 Fubuki著 2025年3月発行, p248)参照)。
また、効果に係る発明特定事項を相違点として認定し、その容易想到性を否定した審決判断が維持された事例として、「免疫原性組成物を安定化させ、沈殿を阻害する新規製剤」事件も挙げられる(2021.06.15ブログ記事「2021.05.17 「メルク・シャープ・アンド・ドーム v. ワイス」 知財高裁令和2年(行ケ)10015」参照)。
しかし本判決は、本件訂正発明9について、「光安定性を向上させる方法」という表現を独立の技術的意義を有する構成とは評価しなかった。裁判所は、「光安定性の向上」は一次包装体に収容することによって通常生じる効果にすぎず、当該一次包装体の「新たな属性」を見出したものではないと判断している。
ここで重要なのは、裁判所が当該効果を「(試験によって)おのずと明らかになる性質」と位置付けた点である。この理解に立てば、本件訂正発明9は、用途発明形式を採ってはいるものの、既存構成に内在する性質を表現したにとどまり、独立の技術的意義を基礎付けるものではないと評価されたことになる。
もっとも、「新たな属性」の有無をいかなる基準で判断するのか、またそれを相違点の容易想到性の問題として整理することの理論的意義について、判決は必ずしも十分に論じていない。内在的性質の単なる認識と、新たな用途の発見との境界をどこに画するのかという問題は、用途発明の成立範囲とも密接に関わる重要論点であり(2022.07.27ブログ記事「「内在同一の問題」 -製薬・バイオテクノロジー分野における新たな科学的発見と公衆衛生との間で揺れる特許保護のジレンマ-」参照)、今後の裁判例の蓄積が待たれるところである。
その意味で、本判決は、「効果の構成化」による形式的差別化に対して一定の限界を示したものと評価できる。
医薬品分野においては、有効性・安全性・品質特性等の向上という効果をいかにクレームに落とし込むかが実務上極めて重要である。本判決は、① その効果が当業者にとって予測困難な質的転換を伴うものか、② それとも規制上当然に実施される試験の結果として把握されるにすぎないものか、を峻別する必要性を改めて示したものといえる。
効果的記載の戦略的活用に対し、より精緻な理論構成と実証的裏付けを求める判断として、実務的示唆は小さくない。
(3)リパスジルをめぐる特許係争の背景
リパスジル(Ripasudil)は、2002年にデ・ウエスタン・セラピテクス研究所(以下「DWTI」)から興和に全世界を対象としてライセンスアウトされ、Rhoキナーゼ(ROCK)阻害薬として開発された緑内障・高眼圧症治療薬である。国内では、2014年9月26日にリパスジル塩酸塩水和物を有効成分とする「グラナテック®点眼液0.4%」として製造販売が承認された。その後、α2作動薬であるブリモニジン酒石酸塩(Brimonidine Tartrate)も配合した「グラアルファ®配合点眼液」が2022年に承認された。
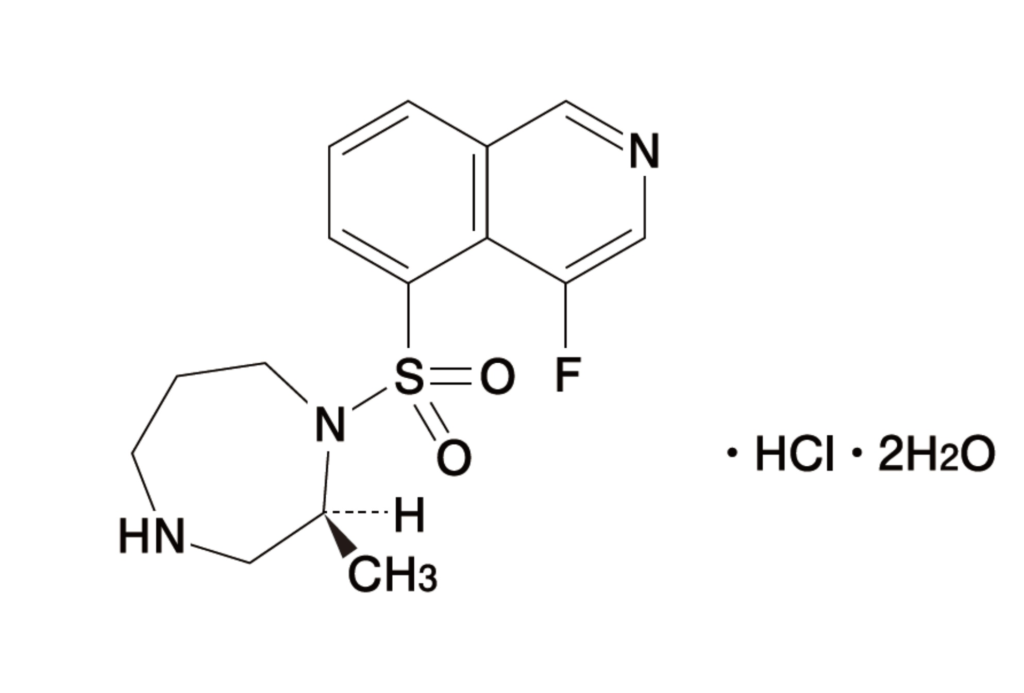 リパスジルは、Rhoキナーゼを阻害することにより房水流出を促進し、眼圧を低下させる薬剤である。従来の緑内障治療薬とは異なる作用経路を有することから、単剤としての使用に加え、他剤との併用療法においても一定の位置付けを占めてきた。
リパスジルは、Rhoキナーゼを阻害することにより房水流出を促進し、眼圧を低下させる薬剤である。従来の緑内障治療薬とは異なる作用経路を有することから、単剤としての使用に加え、他剤との併用療法においても一定の位置付けを占めてきた。
リパスジルの製造販売元である興和は非上場企業であるため、製品別の売上高は公表されていないが、創薬元であるDWTIのIR資料から、その売上動向を概観することができる。リパスジル単剤製剤であるグラナテック®は、2014年の上市から約10年が経過し、国内市場では成熟期に入っている。日本については2024年9月に興和からDWTIへのグラナテック®に関するロイヤリティ受領期間が終了した。興和における国内売上規模は、ピーク時で年間約80億円程度と推計されている。一方、ブリモニジンとの配合剤であるグラアルファ®は近年普及が進んでおり、2024年12月期のDWTI決算資料では、同製品に係るロイヤリティ収益が前期比約75%増と大きく伸長していることが示されている。
グラナテック®点眼液については、承認日である2014年9月26日から2022年9月25日までの8年間が再審査期間として設定され、その終了後、2024年2月15日には、「リパスジル点眼液0.4%『KOG』」(興和AGファーマ)がAG(オーソライズド・ジェネリック)として承認されている。現時点で薬価収載はされていないようである。
リパスジルに関する延長された物質発明の特許権はすでに存続期間を満了している(特許第3834663号及び特許第4316794号)。
また、2026年2月13日、興和は、DWTIと連名で「謹告 リパスジル塩酸塩に関する特許権について」と題する告知文を同社ウェブサイトに掲載した(2026.02.13ブログ記事「リパスジル塩酸塩に関する特許権について」参照)。
当該謹告において、リパスジル塩酸塩水和物が、DWTIにより創出され、興和が「グラナテック®点眼液 0.4%」として製造販売している医薬品であることが改めて明示されている。その上で、リパスジル塩酸塩に関して、以下の特許権がいずれも有効に存続していることが列挙されている。
- 有効成分に関する特許権:特許第4016060号(興和及びDWTI共同所有)、特許第5819705号(興和単独所有)
- 有効成分の製造方法に関する特許権:特許第5858917号、特許第5977289号
- 有効成分を含む製剤に関する複数の特許権:特許第4099201号、特許第4168071号、特許第6236166号、特許第6236167号、特許第6244038号、特許第6452367号、特許第6483632号、特許第6704720号、特許第6704721号、特許第6886322号、特許第6946396号、特許第7137677号、特許第7522817号、特許第7595233号、特許第7635471号、特許第7663792号、特許第7783945号、及び特許第7796937号
さらに、興和及びDWTIは、これらの特許権を含むリパスジル塩酸塩関連の知的財産権について、侵害行為又は侵害のおそれのある行為に対しては直ちに厳正な法的措置を講じる方針を明示している。その上で、リパスジル塩酸塩を含有する医薬品の製造、販売、輸入等を計画する企業に対し、権利侵害が生じないよう十分留意するよう注意喚起を行っている。
なお、謹告文に掲載された特許群の一つである特許第6236167号については、無効審決を支持する知財高裁判決(令和7年(行ケ)第10051号)が2026年1月22日に言い渡されている。この判決は、製剤発明における点眼容器材質選択についての進歩性判断が争点となった事案であり、リパスジル点眼液0.4%の後発医薬品参入のタイミングにも一定の影響を及ぼす可能性がある(2026.02.02ブログ記事「2026.01.22 「興和 v. 東亜薬品」 知財高裁令和7年(行ケ)10051 ― リパスジル製剤特許、点眼容器材質選択と進歩性をめぐる審決取消訴訟」参照)。

そして、本件特許第6244038号も、謹告文に掲載された特許群の一つであった。
実際、現時点では、東亜薬品は、併用剤特許ではなく、特定の製剤特許に対してのみ無効審判を請求していることから、他の製剤特許等の発明の技術的範囲を回避しつつ、単剤であるリパスジル点眼液0.4%の市場参入を狙っているように思われる(2026.02.02ブログ記事「2026.01.22 「興和 v. 東亜薬品」 知財高裁令和7年(行ケ)10051 ― リパスジル製剤特許、点眼容器材質選択と進歩性をめぐる審決取消訴訟」参照)。

これに対し、グラアルファ®配合点眼液は、リパスジルにブリモニジンを組み合わせた配合剤であり、2022年9月26日に製造販売承認を取得している。本剤の再審査期間は6年間とされ、2028年9月25日まで継続する。この再審査期間中は後発医薬品の承認申請が制限されるため、同配合点眼液の後発医薬品は事実上参入することはできない。
現時点では、リパスジル点眼液0.4%AG以外の後発医薬品の承認は確認されていないものの、先発メーカー側がAG承認に踏み切っている経緯を踏まえると、リパスジル点眼液0.4%については、今後、非AGを含む後発医薬品の承認が進み、先発医薬品と後発医薬品が併存する市場構造へと移行する可能性が高いと考えられる。
※ご覧いただきありがとうございます。この記事の内容について、読者の皆さまのご意見や気づきもぜひお聞かせください!
以下のようなご感想・質問、大歓迎です!
- 🤔ここ理解しづらいな、という部分はありましたか?
- 🤔このニュース、事件、判決例の実務影響についてご意見ありますか?
- 🤔過去の類似事例や判決例をご存じでしたら教えてください!
- 🤔恥ずかしい質問、つぶやき、大歓迎です
- 「👍」「なるほど」「疑問あり」だけでもOK!
コメント欄は↓ コメントは匿名OK! ぜひ気軽に投稿してください🙇
皆さんの反応が、次回の記事や解説のヒントになります🥰
Robot icons created by Freepik – Flaticon; Robot cat icons created by Freepik – Flaticon





コメント